Puntos clave
- El virus del papiloma humano (VPH) se divide en tipos de alto riesgo y de bajo riesgo según su oncogenicidad.
- La infección por VPH es condición necesaria pero no suficiente para el desarrollo de cáncer de cuello de útero. Otros factores de índole socioeconómico y de hábitos sexuales se han visto relacionados con el desarrollo tumoral. El preservativo es factor protector.
- No existe aún ningún estudio que haya podido evaluar la posibilidad de que la vacuna disminuya la probabilidad de padecer cáncer de cuello de útero. Sí ha demostrado disminuir la aparición de CIN-1 y CIN-2, viéndose notablemente reducida la magnitud del efecto al analizar los datos de disminución de CIN-3.
- Los datos de seguridad publicados de acuerdo con los ensayos clínicos aleatorizados (ECA) no han encontrado efectos adversos graves atribuibles a la vacuna. Sin embargo, los datos procedentes de registros de farmacovigilancia muestran un número de episodios adversos (leves y graves) notablemente superior al resto de vacunas comercializadas.
- La relación coste-efectividad de la vacuna dependerá de la necesidad de revacunación, la disminución de los costes y el mantenimiento de buenos programas de diagnóstico precoz mediante citología y detección de VPH.
- Existen múltiples incógnitas que despejar en torno a esta vacuna, especialmente en relación con la duración de su protección, los efectos en mujeres previamente infectadas y la posible inmunidad cruzada.
- El coste de oportunidad de la introducción de la vacuna del VPH en el calendario de vacunaciones de España es elevado, especialmente en un momento de crisis económica en el que la «disponibilidad a pagar» del sistema sanitario puede verse reducida.
- Sería deseable desarrollar estrategias de abordaje de los problemas de salud de la mujer desde una perspectiva más amplia, sin caer en reduccionismos microbiológicos que pueden incrementar las desigualdades y obviar aspectos importantes de los problemas que se quieren solucionar.
¿Qué es y qué lesiones produce el virus del papiloma humano?
El virus del papiloma humano (VPH) es un virus ADN. Su capacidad para infectar se debe a su tropismo por piel y mucosas, principalmente mediante transmisión sexual, causando diferentes lesiones: verrugas vulgares y genitales; cáncer de cuello de útero, ano, genitales externos y orofaríngeo; papilomatosis respiratoria recurrente, etc.
Algunos tipos de VPH tienen potencial oncogénico, pudiendo clasificarse en:
1. Bajo riesgo de malignidad: principalmente tipos 6 y 11, implicados en las verrugas genitales.
2. Alto riesgo de malignidad: sobre todo los tipos 16, 18, 31, 51, 52, 53 y 66, implicados en el cáncer de cuello de útero.
En la aparición de lesiones malignas, se contemplan cuatro eventos fundamentales:
1. Adquisición del VPH.
2. Persistencia de la infección.
3. Progresión hacia una lesión precancerosa (neoplasia intraepitelial cervical [CIN]; grados 1, 2 y 3, este último considerado carcinoma in situ).
4. Invasión local.
En la tabla 1 se exponen algunos datos epidemiológicos de interés. Destaca que en España, comparado con otros países, la prevalencia tanto de infección como de cáncer de cuello de útero o la mortalidad por dicho cáncer es baja. También se observa que la mayor parte de los tipos involucrados en las infecciones no están cubiertos por las vacunas, que la mayoría de las infecciones no son persistentes y que en gran porcentaje no evolucionan a displasias ni a cáncer.

¿Qué hay detrás de las lesiones por virus del papiloma humano?
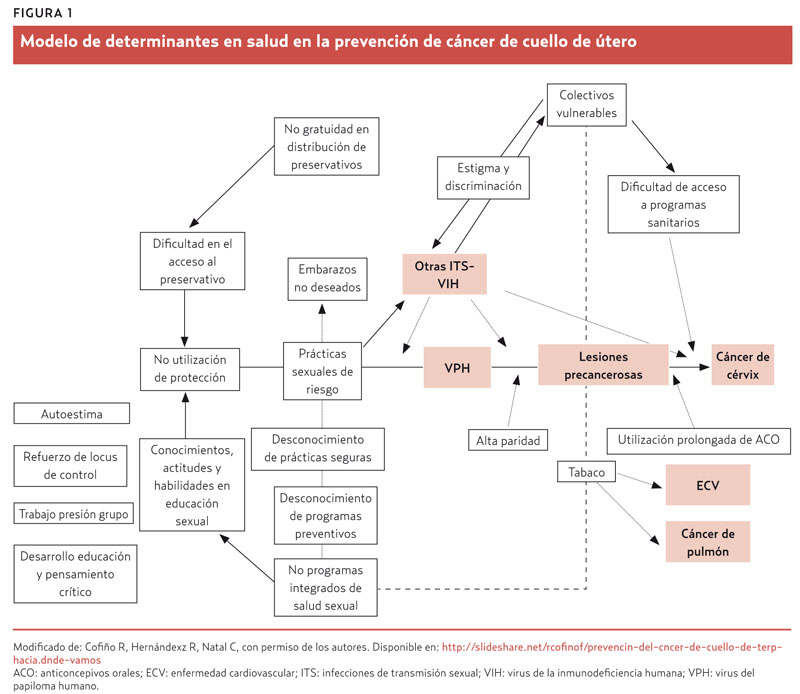
La infección persistente (más de 12 meses) por alguno de los 15 tipos oncogénicos es condición necesaria pero no suficiente para la aparición de displasia y cáncer de cuello de útero. Múltiples estudios han analizado la influencia de otros factores (figura 1)1-3:
• Multiparidad (cinco o más alumbramientos).
• Uso de terapia hormonal más de 5 años.
• Mantener sexo con hombre que haya tenido seis o más parejas sexuales.
• Coinfección por C. trachomatis y virus herpes simple tipo 2 (VHS-2).
• Nivel socioeconómico bajo.
• Déficit de micronutrientes.
• Tabaquismo.
• Comienzo de relaciones sexuales a edades tempranas.
• No utilizar preservativos.
• Pertenecer a algunos grupos sociales marginales (prostitutas, adictas a drogas o a alcohol, reclusas y portadoras del virus de la inmunodeficiencia humana [VIH]).
Vacuna del virus del papiloma humano: ¿qué es y para qué se supone que sirve?
Existen dos vacunas comercializadas: la tetravalente (VPH-4, frente a tipos 6/11/16/18), y la bivalente (VPH-2, tipos 16/18). Ambas son recombinantes: están compuestas por partículas semejantes a virus (VLP), formadas por las proteínas L1 de las cápsulas de los VPH, y utilizan sales de aluminio como adyuvante.
Las dos vacunas están aprobadas a partir de los 9 años de edad para la prevención de lesiones genitales precancerosas (cervicales, vulvares y vaginales) y cáncer cervical. La versión VPH-4 también está indicada para la prevención de verrugas genitales.
Su acción está mediada por una doble respuesta inmunitaria: humoral, y en menor grado, celular. Parece que esta última es responsable, en parte, de la protección cruzada frente a otros tipos víricos y de la inmunidad a largo plazo4.
¿Para qué ha demostrado servir realmente la vacuna?
No existe hasta la fecha ningún ensayo clínico aleatorizado (ECA) que haya evaluado la protección de las vacunas frente al cáncer, pues se necesitan décadas para que una displasia evolucione, si lo hace, a cáncer invasivo, de modo que se precisarían ECA con poblaciones grandes y a largo plazo. Por eso, la comercialización de las vacunas se aprobó según su impacto sobre variables subrogadas (lesiones displásicas) no siempre válidas para predecir resultados en salud (incidencia y mortalidad por cáncer de cuello de útero).
Para interpretar los resultados de los ECA existentes, es necesario considerar tres aspectos:
1. Buscar datos analizados con intención de tratar. Parte de la complejidad de los ECA sobre vacunas del VPH recae en sus distintos modos de análisis cuyos resultados conllevan interpretaciones dispares. El que mejor remeda la vida real es el análisis por intención de tratar modificado sin restricciones: mujeres que recibieron al menos una dosis (tuvieran o no infección previa), hicieron al menos una visita del protocolo de estudio y cuyos resultados se midieron a partir del primer mes tras la primera dosis.
2. Escoger datos sobre displasias graves. La validez y fiabilidad de las displasias CIN-3 es mejor que las CIN-1 y CIN-2 (su diagnóstico muestra menor variabilidad y predice mejor la evolución a cáncer invasivo).
3. Considerar lesiones provocadas por todos los tipos. Deben examinarse todos los tipos de VPH y no solo los cubiertos por las vacunas5. De lo contrario, se pierde la oportunidad de estudiar si estas reducirán a largo plazo la incidencia de cáncer o solo reemplazarán unos tipos por otros, disminuyendo así su efectividad.
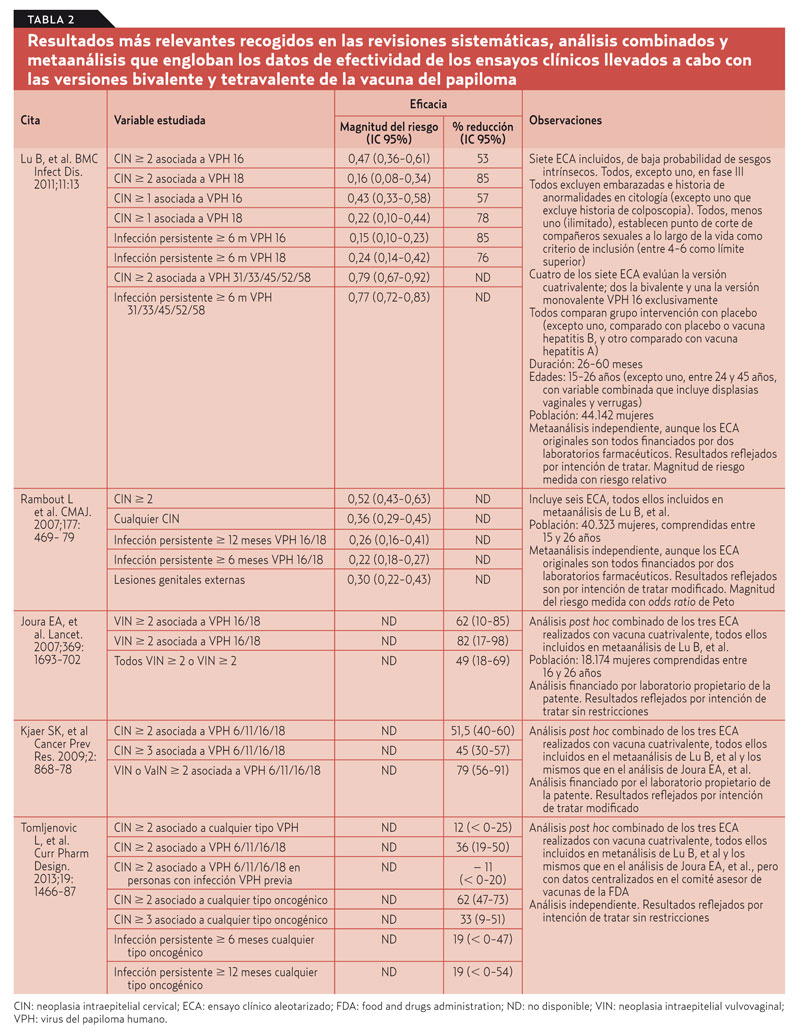
Se han publicado siete ECA englobados en varias revisiones y metaanálisis (tabla 2). Todos aportan porcentajes de resolución de displasias muy altos, también para vulva y vagina. Sin embargo, observando solo resultados clínicamente relevantes (CIN-3 o superior y lesiones asociadas a cualquier VPH), la eficacia disminuye considerablemente y la precisión de los resultados es menor (intervalos de confianza amplios).
Es importante resaltar que la vacunación no sustituye a los programas de detección precoz del cáncer de cuello de útero, por lo que habría que mantenerlos.
¿Es segura?
La mayoría de los ECA concluyen que la vacuna no se asocia a efectos adversos significativos. Sin embargo, en mujeres previamente infectadas se observa una tendencia, no significativa, a aumentar los casos de displasia moderada/grave, aun cuando las infecciones se debieran a tipos incluidos en la vacuna.
Pero para conocer datos sobre seguridad se deben estudiar, además de los ECA, resultados procedentes de sistemas de vigilancia epidemiológica, estudios de cohortes y comunicaciones de casos, pues más del 50% de los efectos adversos de los medicamentos se describen tras su comercialización. Además, se debe revisar la metodología de los análisis estadísticos de los estudios de seguridad, la composición de los placebos en los ECA (contenían sales de aluminio, posible causante de efectos adversos graves) y los procedimientos empleados por los comités de seguridad para evaluar la atribución de los episodios adversos a la vacuna.
En una cohorte de 189.629 mujeres vacunadas con alguna dosis de VPH-4, un comité independiente de seguridad evaluó la posible asociación de la vacuna con episodios adversos, alcanzando significación estadística solo las infecciones en la zona de punción y síncope6. En otro estudio similar con más de 600.000 mujeres, no se alcanzó significación estadística en ningún efecto adverso analizado7.
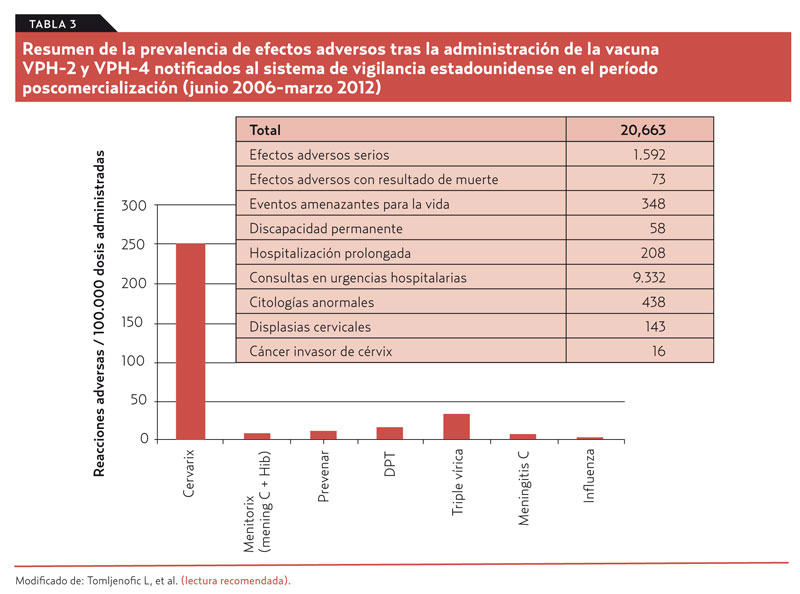
Las bases de datos de efectos adversos, que suponen una importante fuente de datos de seguridad, tienden a estar infrarrepresentadas al depender del grado de notificación voluntaria de los profesionales (vigilancia pasiva). El estadounidense Vaccine Adverse Events Reporting System había recibido en 2,5 años 12.424 notificaciones de efectos adversos (incidencia acumulada de 54 notificaciones por cada 100.000 dosis8). Recientes análisis que incluyen casi 6 años desde el comienzo de la comercialización de las vacunas recogen los datos resumidos en la tabla 3. De todas las vacunas administradas a mujeres de entre 6 y 29 años, la del VPH acapara más del 60 % de las reacciones adversas serias notificadas.
¿Vale la vacuna del virus del papiloma humano lo que cuesta?
Uno de los aspectos más controvertidos es la financiación pública de la vacuna. Los estudios de evaluación económica realizados en países de renta baja o media-baja (con alta prevalencia de cáncer de cuello de útero y débiles programas de detección precoz) tienen resultados más favorables, siendo el beneficio de administrar la vacuna en preadolescentes mayor. En países de renta media-alta los resultados dependerán de cuatro factores que, de cumplirse, mejorarían su relación coste-efectividad9:
1. Que la vacuna confiera inmunidad duradera, evitando la revacunación.
2. Que su coste descienda tras su financiación.
3. Que se logren altas tasas de vacunación.
4. Que se mantengan o mejoren los programas de cribado de cáncer de cuello de útero.
De todos modos, no toda actividad costo-efectiva debe ser financiada. Hay que tener en cuenta el impacto presupuestario de su inclusión en la cartera de servicios y realizar un análisis marginal que permita a los agentes públicos priorizar la financiación de las intervenciones que puedan aportar mayor beneficio.
En España, la vacuna se introdujo por dictámenes políticos, desoyendo recomendaciones técnicas de prudencia por el gran impacto que tendría en el presupuesto de salud pública, sin olvidar que su relación coste-efectividad se basaba en generosos supuestos. Ahora persisten las mismas dudas técnicas, pero políticamente su desfinanciación sería vista como un recorte social, no como una racionalización del gasto.
Cuestiones pendientes sobre la vacuna del virus del papiloma humano
Además de las dudas sobre la seguridad y los beneficios a largo plazo, existen múltiples cuestiones que llaman a la cautela.
• Subgrupos de riesgo. Se desconoce si la efectividad de la vacuna es igual en todas las mujeres o no, lo que daría idea de la necesidad de actuar sobre grupos concretos o sistemáticamente en toda la población. Para ello, los ECA deberían haber estratificado según algunas covariables, por ejemplo, hábitos sexuales; pero, al contrario, los ECA excluían a mujeres con más de 4-5 parejas, precisamente las de mayor riesgo.
• Poblaciones de bajo riesgo. La baja prevalencia de cáncer de cuello de útero e infecciones por VPH en España debe hacer pensar que la eficacia demostrada en los ECA no es directamente extrapolable aquí.
• Infecciones previas. Se sabe que la vacuna no elimina la infección, pero no qué efecto clínico tendría vacunar a mujeres con infecciones previas10. Recientes datos sugieren que esto aumentaría el riesgo de displasia, pudiendo paradójicamente condicionar mayor riesgo de evolución a cáncer de cuello de útero.
• Coinfecciones múltiples. Se desconoce el efecto de la vacuna en mujeres con coinfecciones por múltiples VPH.
• Grupos de edad. Aunque la ficha técnica de ambas vacunas autoriza su administración a partir de los 9 años de edad, los ECA disponibles solo han incluido a mujeres entre 15 y 45 años; en niñas a partir de 9 años únicamente se han realizado estudios de inmunogenicidad. Por otro lado, solo se dispone de un estudio en mujeres entre 25 y 45 años, insuficiente para concluir si la vacuna es eficaz en este grupo de edad donde lo habitual es haber mantenido ya relaciones sexuales y tener, por tanto, más posibilidad de infección.
• Interferencia con otras vacunas y enfermedades. Se desconoce el efecto inmunológico de su administración conjunta con otras vacunas o qué situaciones pudieran disminuir su efectividad, como inmunodeficiencia o enfermedades autoinmunitarias, motivos de exclusión en algunos ECA.
• Relajación de medidas protectoras. La falsa sensación de seguridad al vacunar a escolares y adolescentes podría relajar las medidas preventivas de salud pública, y reducir la efectividad de la vacuna.
• Inmunidad a largo plazo. Hay dudas sobre el mantenimiento de la inmunidad de la vacuna. Los niveles humorales parecen mantenerse altos 9 años, pero más allá solo se dispone de modelos matemáticos. El número de mujeres que se deberán vacunar para evitar un caso de cáncer de cuello de útero variará enormemente según el grado de protección en el tiempo. Se desconoce si serán necesarias dosis de recuerdo o, incluso, si serían suficientes dos dosis iniciales en vez de tres. También se desconoce su efecto sobre la inmunidad natural.
• Protección cruzada y de rebaño. Se postula que la vacuna posee potencial de protección cruzada (a tipos no incluidos en la vacuna) y de inmunidad de rebaño (a personas no vacunadas), lo que añadiría beneficios a los mostrados hasta ahora. Sin embargo, parece que el grado de inmunidad cruzada es bastante modesto, quedaría limitado a algunos tipos emparentados filogenéticamente con los 16 y 18 (sobre todo el 31), y se agotaría con el tiempo5. Por otro lado, las evidencias indirectas de inmunidad de rebaño obtenidas al vacunar masivamente a mujeres jóvenes son aún débiles11.
• Reemplazo de tipo. Se ha observado que algunas vacunas sistemáticas pueden provocar desequilibrios en la ecología local de los gérmenes favoreciendo el desarrollo de otros tipos no incluidos en la vacuna. En el caso concreto de la vacuna del VPH los datos parecen contradictorios11,12. En un estudio realizado en mujeres de entre 21-29 años sometidas a citologías, la prevalencia de infecciones por tipos oncogénicos es mayor en las vacunadas frente a las no vacunadas (30,8 frente al 24,4 %), mientras que la de virus 16/18 fue similar en ambos grupos (8,1 frente al 8,7 %)13. Si se confirmara el reemplazo de tipo, habría que estudiar su impacto sobre la incidencia y agresividad de lesiones premalignas y malignas.
• Vacunación escolar. Algunas comunidades autónomas, como Catalunya y Extremadura, han introducido la vacunación en colegios para lograr mayor cobertura. Esto ofrece dudas sobre la autonomía de las escolares y la adecuada obtención del consentimiento informado.
Consideraciones finales
Los determinantes del desarrollo de cáncer de cuello de útero son muchos e incluyen factores sobre los que actuar mediante prevención secundaria y vacunaciones, pero principalmente mediante un fuerte impulso de la promoción de la salud sexual.
Las estrategias de prevención del cáncer de cuello de útero no pueden implementarse desde el reduccionismo microbiológico ni sociológico, sino desde una visión de salud pública y salud sexual de la mujer donde se consideren las causas y se prioricen las intervenciones basándose en una lectura crítica de la evidencia científica, teniendo en cuenta no solo la efectividad y la seguridad de las acciones posibles, sino también sus resultados sobre la equidad y la eficiencia del sistema sanitario y los servicios de protección social.
Agradecimientos
A Laura Jiménez por su diligente labor de configuración editorial.
Lecturas recomendadas
Tomljenovic L, Spinosa JP, Shaw CA. Human Papillomavirus (HPV) Vaccines as an option for preventing cervical malignancies: (How) effective and safe? Curr Pharm Des. 2013;19:1466-87.
Revisión amplia que ahonda en las numerosas cuestiones clave en torno a la eficacia y seguridad de la vacuna, analizadas con ojo crítico y de forma independiente. Aporta datos que habían previamente formado parte de los expedientes de solicitud de registro de las vacunas en las agencias reguladoras, pero que habían sido selectivamente omitidos en las publicaciones oficiales de los ensayos clínicos pivotales.
Martínez-González MA, Carlos S, de Irala J. Vacuna contra el virus del papiloma humano: razones para el optimismo y razones para la prudencia. Med Clin (Barc). 2008;131:256-63.
Texto publicado cuando la vacuna del VPH llevaba poco tiempo comercializada y que plantea dudas que aún no han sido resueltas en estos años, además de abordar algunas cuestiones sobre estrategias de salud pública que deberían ser tomadas en cuenta a la hora de plantear la priorización de las diversas opciones posibles para actuar sobre problemas sanitarios.
Programa de vacunacions de l’Agència de Salut Pública de Catalunya. Comitè Tècnic de Vacunes del Consell Assessor de l’Agència de Salut Pública de Catalunya. La vacunació contra el virus del papilloma humà (VPH) a Catalunya: Actualització 2013. Disponible en: http://www20.gencat.cat/docs/canalsalut/Home%20Canal%20Salut/Professionals/Temes_de_salut/Vacunacions/documents/Arxius/VPH_febrer_2013_actualitzacio.pdf (Consultado el 1/3/2013)
Actualización institucional sobre la vacuna del VPH. Su mayor interés radica en la discusión de algunas evidencias sobre cuestiones de actualidad en torno a la vacuna, como la protección cruzada, la inmunidad a largo plazo y el reemplazo de tipo. Ha sido muy difundido entre los profesionales sanitarios de Catalunya.
Bibliografía
- Grupo de trabajo de la Ponencia de Programa y Registro de Vacunaciones. Virus del papiloma humano: Situación actual vacunas y perspectivas de su utilización [Internet]. Madrid: Ministerio de Sanidad y Consumo. Disponible en: http://www.msc.es/profesionales/saludPublica/prevPromocion/vacunaciones/docs/VPH_2007.pdf (consultado 28/2/2013)
- Brankovi I, Verdonk P, Klinge I. Applying a gender lens on human papillomavirus infection: cervical cancer screening, HPV DNA testing, and HPV vaccination. Int J Equity Health. 2013;12:14.
- Cofiño R. Prevención del cáncer de cuello de útero: ¿hacia dónde vamos? [Internat]. Disponible en: http://www.slideshare.net/rcofinof/prevencin-del-cncer-de-cuello-de-tero-hacia-dnde-vamos
- Lehtinen M, Herrero R, Mayaud P, Barnabas R, Dillner J, Paavonen J, et al. Studies to assess the long-term efficacy and effectiveness of HPV vaccination in developed and developing countries. Vaccine. 2006;24 Suppl 3:S3/233-41.
- Malagón T, Drolet M, Boily MC, Franco EL, Jit M, Brisson J, et al. Cross-protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis. Lancet Infect Dis. 2012;12:781-9.
- Klein NP, Hansen J, Chao C, Velicer C, Emery M, Slezak J, et al. Safety of quadrivalent human papillomavirus vaccine administered routinely to females. Arch Pediatr Adolesc Med. 2012;166:1140-8.
- Gee J, Naleway A, Shui I, Baggs J, Yin R, Li R, et al. Monitoring the safety of quadrivalent human papillomavirus vaccine: Findings from the Vaccine Safety Datalink. Vaccine. 2011;29:8279-84.
- Slade BA, Leidel L, Vellozzi C, Woo EJ, Sutherland A, Izurieta HS, et al. Postlicensure safety surveillance for quadrivalent Human Papillomavirus recombinant vaccine. JAMA. 2009;302:750-7.
- Puig-Junoy, J, González López-Valcárcel B. Economic evaluations of massive HPV vaccination: within-study and between study variations in incremental cost per QALY gained. Prev Med. 2009;48:444-8.
- Hildesheim A, Herrero R, Wacholder S, Rodriguez AC, Solomon D, Bratti MC, et al. Effect of human papillomavirus 16/18 L1 virus like particle vaccine among young women with preexisting infection: a randomized trial. JAMA. 2007;298:743-53.
- Kahn JA, Brown DR, Ding L, Widdice LE, Shew ML, Glynn S, et al. Vaccine-type human papillomavirus and evidence of herd protection after vaccine introduction. Pediatrics. 2012;130:e249-56.
- Palmroth J, Merikukka M, Paavonen J, Apter D, Eriksson T, Natunen K, et al. Occurrence of vaccine and non-vaccine human papillomavirus types in adolescent Finnish females 4 years post-vaccination. Int J Cancer. 2012;131:2832-8.
- Wright TC, Stoler MH, Behrens CM, Apple R, Derion T, Wright TL. The ATHENA human papillomavirus study: design, methods, and baseline results. Am J Obstet Gynecol. 2012;206:1-11.



Luis Emilio 22-06-13
Tema adecuado para ampliar los conocimientos sobre estas vacunas ,mis respetos
Luis Andres 14-05-13
Felicidades, claro, resumido y muy útil. Perfecta la tabla 1. Es un orgullo ser MFyC con personas como vosotros.Salud