Puntos clave
- Una masa escrotal puede permanecer largamente asintomática.
- Las características del dolor, si este se presenta, serán un síntoma clave para la orientación diagnóstica inicial.
- Descartada la torsión testicular dentro del síndrome escrotal agudo, toda masa escrotal puede ser abordada inicialmente desde Atención Primaria (AP).
- Pese a su sencillez de realización, la transiluminación es una técnica de gran utilidad en el abordaje inicial de la masa escrotal.
- La ecografía testicular es la prueba complementaria fundamental en AP para completar el diagnóstico diferencial de una masa escrotal (grado de evidencia A).
- Los marcadores tumorales son muy útiles en el diagnóstico del cáncer testicular, pero su negatividad no excluye su presencia.
- La patología benigna (hidrocele, varicocele y quistes epididimarios) solo requerirá derivación si es muy sintomática o mal tolerada.
¿A qué nos referimos?
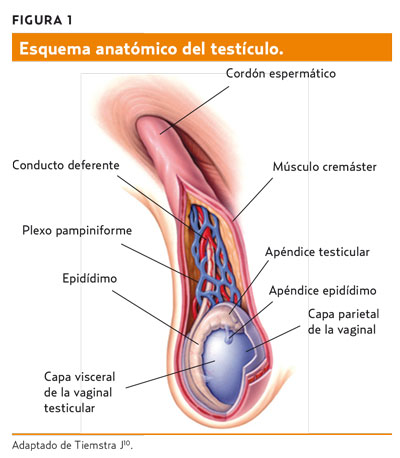 El escroto es una unidad anatómica formada por una bolsa (la bolsa testicular) compuesta por siete capas de las cuales dos son musculares. Engloba a los testículos y sus cordones espermáticos, que a su vez están formados por la arteria testicular (única irrigación del testículo); el plexo pampiniforme, red anastomótica que formará la vena testicular; y el conducto deferente, que une las vesículas seminales al epidídimo testicular. En la figura 1 se muestra el esquema anatómico del testículo.
El escroto es una unidad anatómica formada por una bolsa (la bolsa testicular) compuesta por siete capas de las cuales dos son musculares. Engloba a los testículos y sus cordones espermáticos, que a su vez están formados por la arteria testicular (única irrigación del testículo); el plexo pampiniforme, red anastomótica que formará la vena testicular; y el conducto deferente, que une las vesículas seminales al epidídimo testicular. En la figura 1 se muestra el esquema anatómico del testículo.
Por tanto, una masa o tumoración escrotal es toda aquella estructura expansiva en el escroto que puede o no causar sintomatología. Esta puede detectarse de forma casual por el propio paciente, en una exploración física, o por una prueba complementaria (incidentaloma).
La presentación clínica será fundamental para orientar hacia un grupo de patología, siendo las características del dolor, si existe, la variable de inicio más decisoria a la hora de orientar el estudio. Su presencia de forma aguda marcará la actuación terapéutica, que puede convertirse en una urgencia médica, en cuyo caso habrá que actuar antes de las 6 horas desde el inicio del dolor. Pasado este tiempo, el riesgo de lesión grave testicular puede ser alto, e incluso llegar a ocasionar la pérdida funcional, con la consecuente afectación de la capacidad de reproducción.
Se trataría del denominado síndrome escrotal agudo, de cuya variada etiología destacan tres patologías: la torsión testicular, la orquiepididimitis aguda y la torsión de los apéndices testiculares o hidátides de Morgagni. Estas etiologías forman el 95% del total de las causas; y representan el 35, 30 y 25%, respectivamente, de los diagnósticos en urgencias cuando el motivo de consulta es un dolor escrotal agudo.
Sin embargo, en esta revisión no se abordarán las patologías causantes del síndrome escrotal agudo. Aunque es fundamental en el diagnóstico diferencial de la masa escrotal, la mención de algunos de sus signos clínicos en el apartado de diagnóstico será la única aproximación que se realizará de este síndrome, ya que recientemente ha sido objeto de una actualización en esta misma revista1.
Esta revisión se centrará, pues, en la masa escrotal que presenta una sintomatología subaguda o crónica, o se detecta de forma casual.
¿De qué herramientas diagnósticas disponemos?
Exploración física
En AP, la exploración física será el eje principal para el abordaje diagnóstico de una masa escrotal. La existencia o ausencia de los siguientes signos y síntomas permitirá orientar el estudio y la urgencia del tratamiento. Para obtenerlos habrá que realizar una exploración abdominogenital completa, y detectar la presencia de inflamación, alteraciones dermatológicas u otros efectos masa como la distensión vesical o hernias. En la zona genital, tras una inspección, la palpación bitesticular será obligada, observando su posición y signos orientativos, que suelen estar ausentes en las masas escrotales no agudas:
1. Sintomatología general: presencia de fiebre o síntomas del tracto urinario inferior.
2. Unilateralidad: la mayoría de las patologías tiene una afectación unilateral.
3. Características del dolor: agudo, crónico, leve, tolerancia del paciente, qué lo mejora (la elevación del testículo), qué lo empeora (estar largo tiempo de pie), la existencia de traumatismo previo, etc.
4. Transiluminación: si es positiva, orienta a contenido líquido.
5. Signo de Gouverneur: testículo elevado y horizontalizado. Típico en las torsiones y raro en las patologías infecciosas.
6. Signo de Prehn: mejora del dolor al elevar el testículo. Orienta a patología infecciosa, y es negativo en las torsiones.
7. Signo de Angell: horizontalización del testículo contralateral no afectado. Orienta a torsión testicular.
8. Signo de Ger: difícil de objetivar, se trata de una depresión o invaginación del hemiescroto afectado de una torsión testicular. Aparece previamente al edema escrotal secundario.
9. Reflejo cremastérico: se produce la elevación del testículo por acción de los músculos cremastéricos al raspar con un depresor la cara interna del muslo homolateral. Abolido en la torsión testicular y presente en la torsión de la hidátide de Morgagni.
Exploraciones complementarias
• Hemograma: útil ante la sospecha de proceso infeccioso (leucocitosis) y tumoral/inflamatorio (reactantes de fase aguda como la proteína C reactiva [PCR] y la velocidad de sedimentación globular [VSG]).
• Sedimento de orina: como en el hemograma, ayudará a descartar proceso infeccioso. Su normalidad no descartará patología grave ya que solo un 10% de las neoplasias testiculares cursan con hematuria2.
• Marcadores tumorales: en los tumores testiculares, pueden encontrarse elevados en un 51% de los pacientes, siendo los tumores testiculares no seminomatosos en los que hasta en un 90% se detecta un aumento de uno o dos de ellos. No se debe olvidar, sin embargo, que su negatividad no excluye el diagnóstico de los tumores de células germinales.
Se dispone de los siguientes:
- Alfa-feto-proteína (AFP): elevada en el 50-70% de tumores de las células germinales no seminoma (TCGNS)
- Gonadotropina coriónica humana (HCG): elevada en el 40-60% de los pacientes con TCGNS.
- Lactato deshidrogenasa (LDH): marcador menos específico. Su concentración está muy vinculada al volumen tumoral dada su asociación a la existencia de lisis celular, pudiendo detectarse una elevación significativa en el 80% de los pacientes con neoplasia testicular avanzada.
- Fosfatasa alcalina placentaria (FAPL): de utilidad como marcador de seguimiento de los pacientes con seminoma puro.
Ante la presencia de una masa sólida testicular, la solicitud de AFP, HCG y LDH se considera necesaria, mientras que la FAPL puede ser opcional3 (grado de evidencia A).
• Transiluminación: las masas sólidas no permiten el paso de la luz, mientras que los líquidos sí. Técnicamente, es una prueba sencilla y no precisa una fuente de luz especial, ya que bastará con un haz de luz de potencia media (linterna básica). Será positiva cuando el escroto se hace traslúcido, con un color rojizo-anaranjado; y negativa cuando es opaco. Muy útil para detectar los hidroceles no complicados, espermatoceles y el quiste de cordón espermático, diferenciándolos de las hernias, masas sólidas y hematoceles. Para saber más sobre la técnica, puede consultarse en esta misma revista una práctica explicación4.
• Ecografía: con una sensibilidad del 93,5%, es la prueba fundamental para la indicación de cirugía ante un escroto agudo5 (grado de evidencia B). En el caso de masaescrotal no aguda, permitirá diferenciar entre una masa intratesticular de una extratesticular. Aunque una limitación importante de la ecografía escrotal es que no permite diferenciar entre una masa sólida maligna y una benigna, se recomienda realizarla ante toda masa escrotal con transiluminación negativa, aunque el tumor sea clínicamente evidente3. Sería también aconsejable su realización a pesar de una transiluminación positiva en el caso de un paciente joven y con un valor de HCG o AFP elevada, o en el seguimiento de pacientes con factores de riesgo de neoplasia (tamaño testicular < 12 ml, heterogeneidad de la imagen ecográfica y presencia de microlitiasis). En este último caso, especialmente en pacientes con antecedentes de neoplasia contralateral previa, se debería realizar un seguimiento ecográfico, y recomendar una biopsia testicular si se observan cambios. No obstante, no existe un consenso respecto a la periodicidad del control (anual mayoritariamente) ni a su duración (a los 5 años, hasta un 50% de los pacientes con neoplasia intratubular pueden desarrollar un tumor germinal).
Los falsos negativos de la prueba son raros, con un valor predictivo negativo cercano al 100%.
• Resonancia magnética (RM): la RM escrotal ofrece una mayor sensibilidad (100%) y especificidad (95-100%) que la ecografía para el diagnóstico de tumores6, pero su alto coste no justifica su utilización en AP y debe reservarse a la ampliación de un estudio ante una masa testicular con imagen ecográfica heterogénea.
En qué hay que pensar
Descartado un escroto agudo, las siguientes patologías formarán parte del diagnóstico diferencial:
1. Hernia inguinal: de inicio tórpido, generalmente relacionado con esfuerzo físico agudo o constante como desencadenante. La afectación de la zona inguinal, el aumento de volumen o su palpación en el conducto inguinoescrotal con la práctica de la maniobra de Valsalva orienta hacia su diagnóstico.
2. Hidrocele: colección de líquido peritoneal situada entre la capa visceral y parietal de la túnica vaginal. De consistencia blanda, excepto si se encuentra a tensión. La transiluminación positiva casi confirmará el diagnóstico pudiendo reducir la ansiedad prediagnóstica del paciente. Mayoritariamente son idiopáticos, aunque pueden ser reactivos a infecciones escrotales, cirugía u otras patologías regionales, como neoplasias testiculares. Su presentación clínica es una hinchazón escrotal, y como no son patológicos per se, solo se tratan cuando causan molestias o infección. Su tratamiento es la extirpación quirúrgica, ya que la simple aspiración suele ir seguida de una rápida recidiva7.
3. Varicocele: se trata de una dilatación del plexo venoso pampiniforme localizada cranealmente al testículo. La mayoría son unilaterales izquierdos debido a la peculiar desembocadura de la vena espermática izquierda en la vena renal, que puede causar un incremento de la presión haciendo claudicar, por incompetencia, el sistema valvular venoso. Clínicamente, se expresan como una sensación de peso en el teste afectado, sobre todo en bipedestación, palpándose una masa de venas dilatadas (tradicionalmente comparada al tacto con una bolsa de gusanos, etc.) que aumenta con la maniobra de Valsalva y desaparece o disminuye con el decúbito. Puede ser bilateral en un 33% de los casos, mientras que la afectación unilateral derecha es rara y suele ser signo de patología más grave, secundaria a una obstrucción de la vena cava inferior (trombosis de la vena renal derecha, neoplasia renal trombosada, etc.). En este caso, aparte de la ecografía testicular (con Doppler para valorar los flujos sanguíneos), se aconseja la realización de una ecografía abdominal complementaria. Aunque puede causar atrofia testicular, secundaria a muerte celular por un aumento de la temperatura escrotal asociada, la relación varicocele/infertilidad todavía no está clara. La indicación de tratamiento (la ligadura quirúrgica suele ser la primera opción) dependerá de la sintomatología y la edad: niños con crecimiento retardado, jóvenes infértiles o atrofia testicular y adultos muy sintomáticos. La mayoría de los estudios muestran una mejora de la calidad del semen postratamiento. En el resto de casos se aconseja tratamiento farmacológico con antinflamatorios no esteroideos (AINE) y soporte testicular7 (suspensorio).
4. Quiste epididimario y espermatocele: en la cabeza del epidídimo suelen aparecer quistes simples benignos, derivados de restos embrionarios o ectasias de los conductos de transporte de los espermatozoides. Se diferencian por el tamaño: los espermatoceles son quistes epididimarios mayores de 2 cm. Su diagnóstico es clínico, aunque suelen ser asintomáticos y al palparse externamente a los testículos permiten diferenciarlos de los hidroceles. Si existen dudas, la ecografía suele ser suficiente para completar el diagnóstico. Excepcionalmente, requieren tratamiento.
5. Tumores testiculares: relativamente raros son, sin embargo, los tumores sólidos más frecuentes entre los 15 y 35 años, que constituyen, no obstante, una de las neoplasias más curables. Normalmente, en un principio se observa una masa escrotal indolora, pero en algunos casos se presentan con dolor agudo, resultado de un infarto o hemorragia intratumoral, o bien de una torsión testicular. Con transiluminación negativa, la ecografía escrotal es la técnica diagnóstica de elección, que alcanza una sensibilidad cercana al 100% (grado de evidencia A).El diagnóstico diferencial ecográfico se presenta ante hematomas, infartos testiculares o ectasia tubular. En estos casos, la RM será de gran utilidad.
En un 90-95% de los casos se trata de tumores de células germinativas (seminoma, carcinoma embrionario, coriocarcinoma, tumor del saco vitelino y teratoma). El 5% restante se reparte entre los tumores de los cordones sexuales/estroma gonadal (tumor de células de Leydig y tumor de células de Sertoli, principalmente) y mixtos. La criptorquidia, el síndrome de Klinefelter y los antecedentes familiares de primer grado de tumores testiculares son los principales factores de riesgo8.
6. Tumores de epidídimo y paratesticulares: son raros y habitualmente no son malignos. Se reconocen mediante palpación del escroto, como pequeñas masas epididimarias duras y tensas. La forma de presentación más frecuente es el adenoma quístico, que, en un tercio de los casos, es bilateral. Estos últimos acompañan con frecuencia al síndrome de Von-Hippel-Lindau.
7. Patología dermatológica:
• Quistes dérmicos: de afectación más frecuente en el adulto. Son móviles y se palpan en la dermis, lo que permite diferenciarlos de los nódulos testiculares o epididimarios. Si se infectan, el riesgo de extensión local es alto dada la presencia de abundantes folículos pilosos. Suelen ser de color blanco-amarillento y afectan a cualquier parte de la superficie cutánea del escroto y del cuerpo del pene.
• Edema escrotal idiopático: edema e inflamación de la piel escrotal sin afectación testicular. De causa desconocida, y sin tratamiento efectivo, suele desaparecer de forma espontánea y gradual.
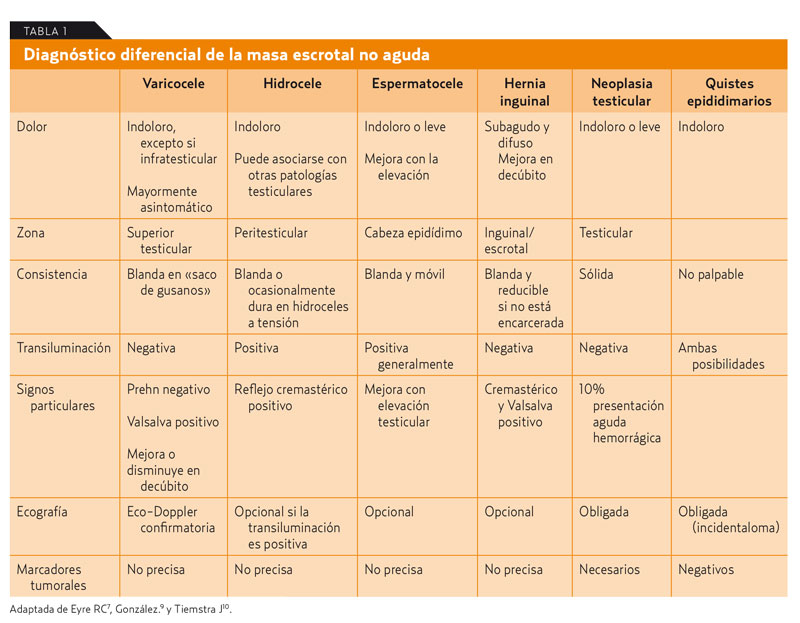
En la tabla 1 se resumen las características del diagnóstico diferencial.
¿Qué hay y qué no hay que derivar? Tratamiento desde la Atención Primaria
Descartado el síndrome testicular agudo, en el que siempre se debe valorar el tratamiento urgente, el abordaje de la masa escrotal no aguda puede realizarse perfectamente en AP, sobre todo en los casos con índice de sospecha de malignidad bajo, y así evitar derivaciones innecesarias al siguiente nivel de especialización. Las hernias inguinales indirectas en general son palpables y solo son una urgencia quirúrgica si se sospecha estrangulación. Además del tratamiento de las lesiones dermatológicas, las patologías benignas como el hidrocele y el varicocele serán tributarias de seguimiento y tratamiento sintomático en AP, siempre y cuando la tolerancia clínica del paciente sea buena y no existan complicaciones. Los quistes epididimarios y los espermatoceles no necesitarán seguimiento continuo ni tratamiento específico7. El resto de patologías, como las hernias inguinales y las neoplasias testiculares, requerirán derivación al siguiente nivel de especialización para un abordaje quirúrgico o médico más específico, que no se detalla porque está fuera del ámbito de interés en el enfoque de este artículo.
En la figura 2 se muestra el algoritmo diagnóstico y de atención propuesto.

Bibliografía
- Llobet Pareja A, Pou Vila R. Escroto agudo. AMF. 2013;9(9):519-22.
- Barnhouse K, Powers A. How should you further evaluate an adult with a testicular mass? J Fam Pract. 2007;56(10):851-3.
- Albers P, Albrecht W, Algaba F, Bokemeyer C, Cohn-Cedermark G, Fizazi K, et al. Guidelines on Testicular Cancer. Eur Urol. 2008 Mar;53(3):478-96, 497-513. Actualización: Eur Urol. 2011 Aug;60(2):304-19.
- Bugarín González R, Blanco Parra M. Realización de una transiluminación escrotal. AMF. 2010;6(9):505-7.
- Andipa E, Liberopoulos K, Asvestis C. Magnetic resonance imaging and ultrasound evaluation of penile and testicular masses. World J Urol. 2004;22:382-91.
- Cassidy FH, Ishioka KM, McMahon CJ, Chu P, Sakamoto K, Lee KS, Aganovic L. MR imaging of scrotal tumors and pseudotumors. Radiographics [Internet]. 2010 May;30(3):665-83. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/20462987
- Eyre RC. Evaluation of nonacute scrotal pathology in adults. En: Rose BD, ed. UpToDate [online database]. Version 14.1. Waltham, Mass: UpToDate; 2013.
- Pérez León N, Pimienta Escrihuela M. Patología uretroescrotal. Scrot Ap Módulo 2. Edición 2012-2013.
- González Santamaría P, Carrodeguas Santos L, Pérez Varela L. Masas escrotales. Guía Fisterra [Internet]. 2012. Disponible en: http://www.fisterra.com/guias-clinicas/masas-escrotales/
- Tiemstra J, Kapoor S. Evaluation of Scrotal Masses. Am Fam Physician. 2008;78(10):1165-70.