Nuevos fármacos
NALOXEGOL (Moventig©)
Introducción
El naloxegol es un derivado pegilado del antagonista del receptor opioide µ naloxona. Se une a los receptores específicos del tracto gastrointestinal y su acción sobre el sistema nervioso central (SNC) es mínima. Su comparador natural es la metilnaltrexona, que tiene el mismo mecanismo de acción.
Indicación
Tratamiento del estreñimiento inducido por opioides (EIO) en pacientes adultos que no responden a los laxantes de la práctica clínica habitual. Debido a su coste, la financiación pública está restringida a pacientes oncológicos y precisa visado de inspección.
Posología
Un comprimido de 25 mg al día con el estómago vacío, 30 minutos antes del desayuno o 2 horas después del mismo. En la insuficiencia renal con FGC < 60 mil/min la dosis inicial es de 12,5 mg al día. No está recomendado en la insuficiencia hepática grave.
Eficacia
Basada en dos ensayos clínicos aleatorizados (ECA) pivotales en fase III, doble ciego y controlados con placebo, de 12 semanas de duración. Se realizaron en pacientes no oncológicos con estreñimiento inducido por opioides (EIO). Se observó un efecto sobre el estreñimiento consistente y con significación estadística con la dosis de 25 mg/día. La mejoría solo se observó entre los pacientes que no respondían a los laxantes habituales. No existe un ensayo clínico (EC) realizado con pacientes oncológicos, pero se supone, fisiopatológicamente, que su respuesta será similar a la de los no oncológicos. Tampoco se dispone de ningún ensayo clínico aleatorizado (ECA) con comparación directa frente a otros laxantes habituales1.
Seguridad y tolerabilidad
En general, no se detectaron efectos adversos graves y los más frecuentes fueron gastrointestinales y cefalea. No interfirió con la analgesia y no se detectaron síntomas claros de abstinencia a opioides. Está contraindicado con inhibidores potentes de la CYP3A4 (claritromicina, ketoconazol, itraconazol, inhibidores de proteasa, etc.). Con inhibidores moderados de la CYP3A4 (diltiazem, verapamilo, etc.) se debe reducir la dosis a 12,5 mg/día.
Coste
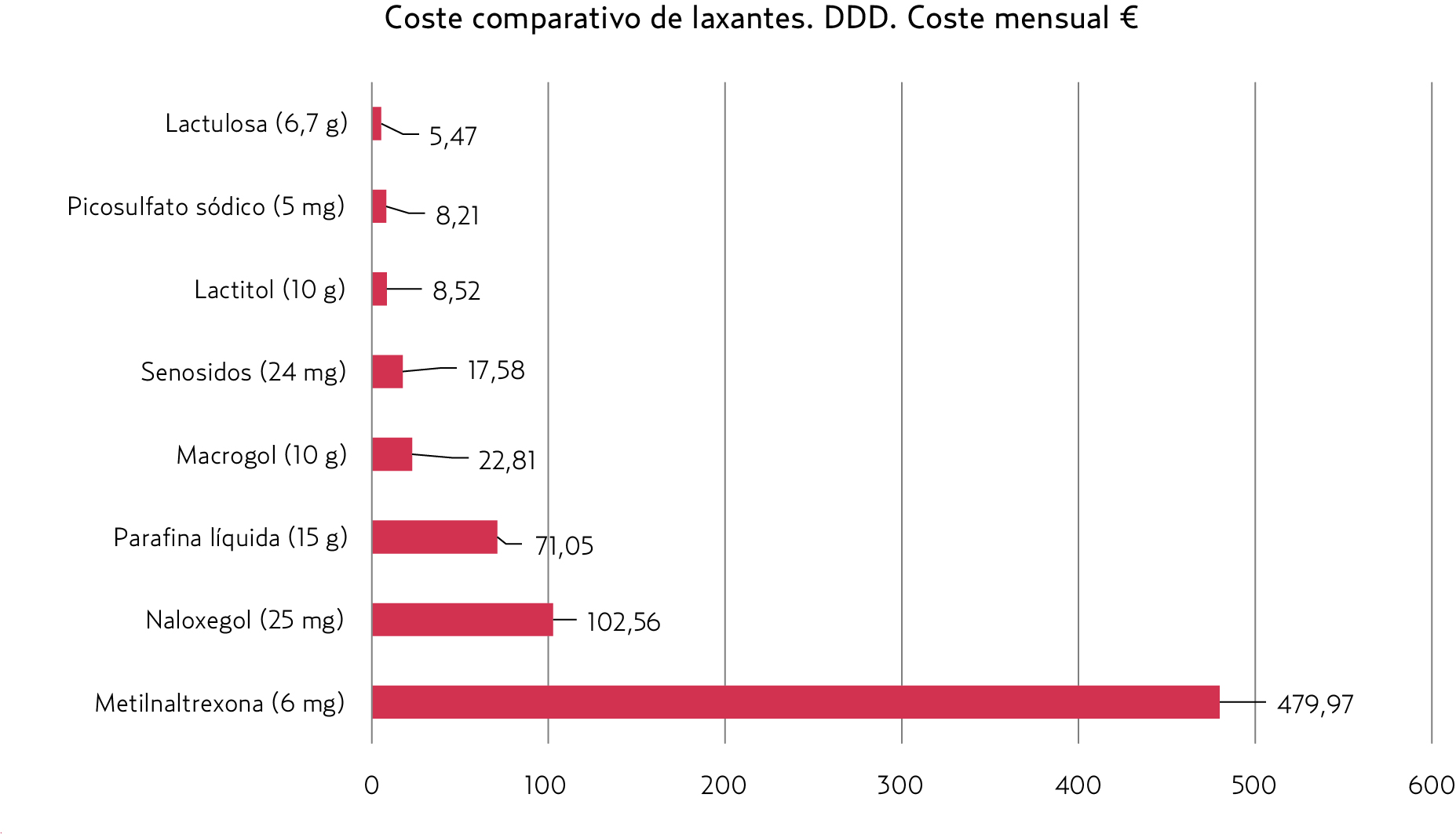
Es un fármaco de coste claramente superior al de los laxantes de la práctica clínica habitual (figura 1). La caja de 30 comprimidos de 25 mg cuesta 102,56 euros.
|
Figura 1. Coste comparativo de laxantes. Fuente: BOT Plus 2.0-. Noviembre 2017 |
 |
Lugar en la terapéutica
La información aún es insuficiente para valorar su lugar terapéutico, pero puede ser una opción de tratamiento oral en pacientes con EIO que no hayan respondido a la terapia laxante habitual. En estos casos puede ser superior a la metilnaltrexona por su coste menor y su uso por vía oral.
Ampliar la información
Comité de evaluación de nuevos medicamentos. Osakidetza. Cevime. 2017; n.º 248. Naloxegol. Disponible en: http://www.osakidetza.euskadi.eus/contenidos/informacion/medicamentos_atencion_primaria/es_def/adjuntos/N/naloxegol_fitxa.CA.pdf
INSULINA glargina 300 U/ml (Toujeo©)
Introducción
La insulina basal glargina 100 U/mL se utiliza desde hace años en la terapéutica de las diabetes mellitus de tipos 1 y 2 (DM 1 y DM 2). Más recientemente, se ha aprobado y comercializado la presentación de insulina glargina en la concentración de 300 U/mL confiriéndole unas características distintas que conviene destacar.
Indicación
Es una insulina basal para administrar una vez al día y, debido a que no tiene pico de acción y su duración es claramente superior a 24 horas, se puede utilizar a cualquier hora del día, pero preferiblemente alrededor de la misma hora cada día. Está aprobada para utilizarla en > 18 años por falta de estudios a edades menores. Se administra solo con plumas precargadas Solostar©, por lo que no hay posibilidad de error porque así se administran unidades de insulina y no se mide el volumen, que será un tercio del administrado con glargina 100 U/mL con la misma cantidad de unidades.
Posología
Esta insulina se puede administrar hasta 3 horas antes o después de la hora de uso habitual. Para pacientes con DM 2, la dosis inicial recomendada es de 0,2 U/kg/día, seguida de los ajustes necesarios.
El estado estacionario en el intervalo terapéutico se alcanza después de 3-4 días de la administración de esta insulina. Tras la administración subcutánea, la variabilidad intrapaciente, definida como el coeficiente de variación en la exposición a insulina durante 24 horas, fue baja en el estado estacionario (17,4 %).
Cambio de insulina glargina 100 U/mL a Toujeo©: no son bioequivalentes por su comportamiento farmacodinámico distinto y no son directamente intercambiables. En principio, el cambio puede hacerse unidad a unidad, pero luego será necesario hacer ajustes y habitualmente se necesitan dosis más altas de Toujeo© (entre 10-18 %). Cambio de Toujeo© a insulina glargina 100 U/mL: la dosis debe reducirse aproximadamente un 20 %.
Cambio de otras insulinas basales a Toujeo©: si se utiliza una insulina basal una vez al día, se puede cambiar unidad a unidad en función de la dosis de insulina basal previa. Según los controles posteriores, habrá que ajustar las dosis de la insulina basal o de Toujeo© o de las insulinas rápidas, si se utilizan, y de los fármacos antihiperglucémicos no insulínicos. Al cambiar de insulina basal dos veces al día a Toujeo© una vez al día, la dosis inicial debe ser el 80 % de la dosis diaria total de la insulina basal previa.
Eficacia y seguridad
El efecto hipoglucemiante de Toujeo© es más estable y prolongado que el de la insulina glargina 100 U/mL. Toujeo© dura siempre más de 24 horas (hasta 36 horas) (figura 2).
|
Figura 2. Perfil de la actividad en estado estacionario en pacientes diabéticos de Toujeo© vs. insulina glargina 100 U/mL |
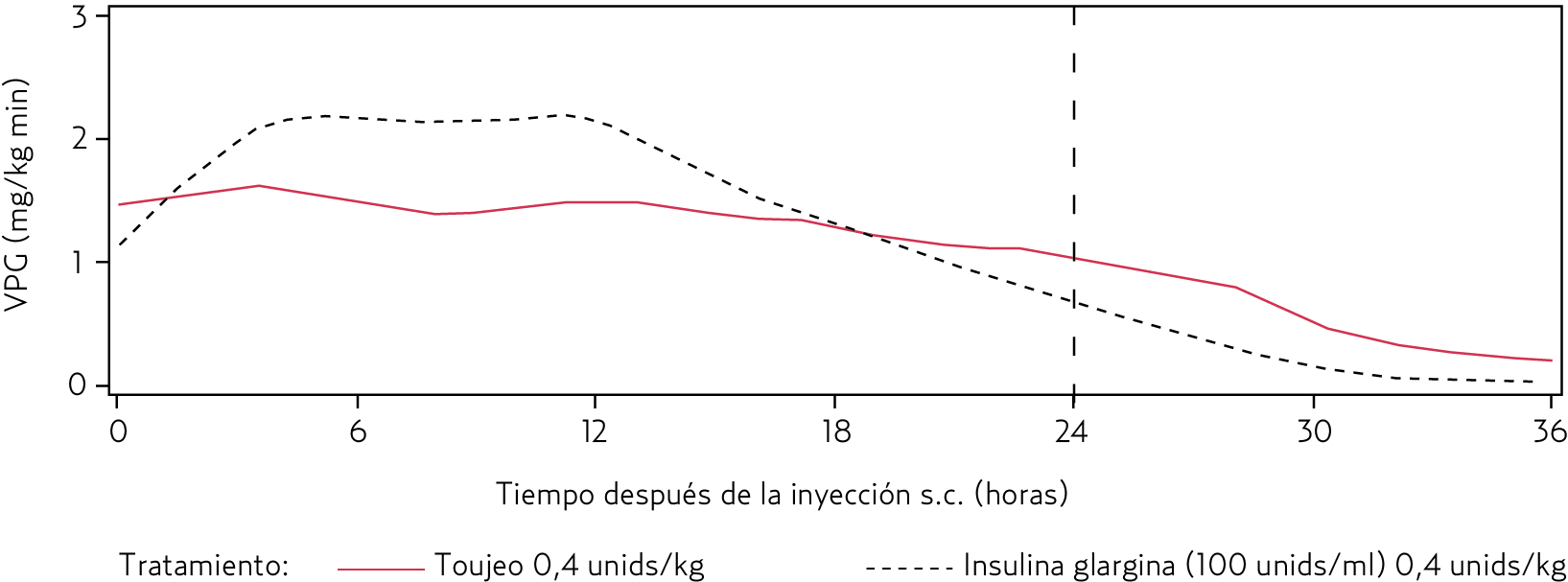 |
El perfil de acción más regular y duradero de Toujeo© se atribuye a la reducción del volumen de la inyección en dos tercios, lo que da como resultado una superficie de precipitado más pequeña.
En diversos ECA, con 546 personas con DM 1 y 2474 con DM 2 y duración de los estudios hasta 26 semanas, la eficacia sobre el control glucémico fue similar entre ambas presentaciones de insulina glargina, tanto en pacientes con DM 1 como con DM 2. El control fue similar utilizando Toujeo© tanto por la mañana como por la noche. Las dosis necesarias de Toujeo© fueron un poco superiores (10-18 %) que las de glargina 100 U/mL2.
La incidencia de hipoglucemias confirmadas fue inferior en los pacientes con DM 2 tratados con Toujeo© respecto a los controlados con glargina 100 U/mL. La reducción de hipoglucemias fue a lo largo del día y por la noche. En los pacientes con DM 1 las hipoglucemias fueron similares con ambas presentaciones de insulina glargina3.
Tanto la mejoría del control glucémico como del número de hipoglucemias fue independiente de edad, el sexo, el índice de masa corporal (IMC) y la duración de la diabetes.
La ganancia de peso fue pequeña y menor que con la insulina glargina 100 U/mL, pero sin clara significación estadística4.
Toujeo© puede emplearse durante el embarazo y la lactancia.
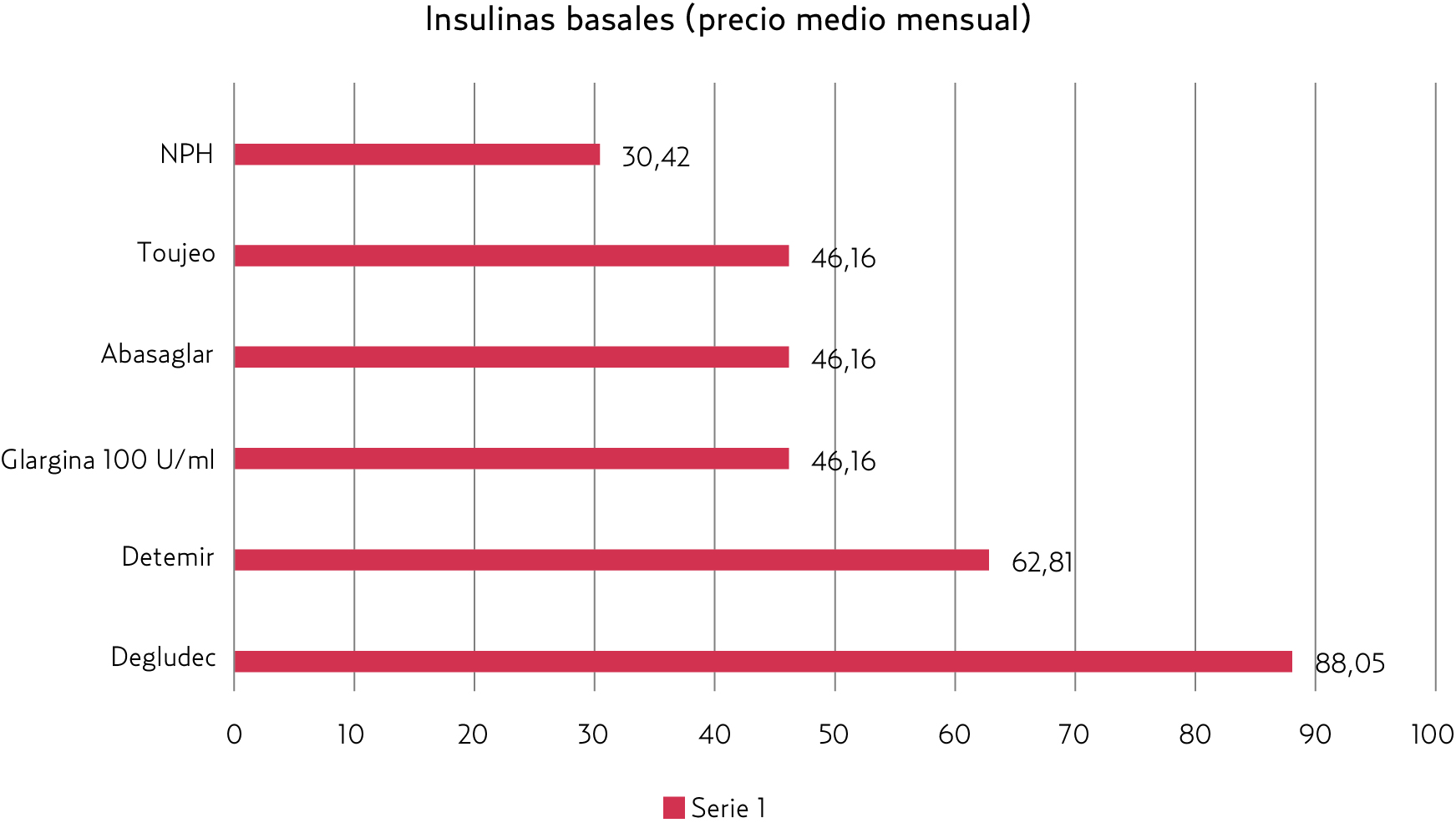
Coste (figura 3)
|
Figura 3. Insulinas basales, precio (€) medio mensual con una dosis diaria de 40 unidades |
 |
Lugar en la terapéutica
La insulina glargina 300 U/mL Toujeo© permite una acción hipoglucemiante más prolongada y regular que la concentración de insulina glargina 100 U/mL, con menor número de hipoglucemias y un control glucémico similar. Su duración, claramente superior a 24 horas, permite administrarla a cualquier hora del día, aunque el horario de cada día debe ser similar (se permite una variación de +/- 3 h). Estas ventajas son a un coste similar que la concentración habitual de insulina glargina.
En diabéticos con resistencia insulínica (definida por el uso de insulina > 200 U/día o > 2 U/kg/día) o los que se administran dosis diarias elevadas de insulina, se pueden beneficiar del mismo número de unidades con solo un tercio de volumen, lo que disminuye las molestias y complicaciones locales.
Ampliar la información
Ficha técnica de insulina glargina 300 U/mL Toujeo©. https://cima.aemps.es/cima/pdfs/es/ft/100133034/FT_100133034.pdf
TRAMADOL/DEXKETOPROFENO (Enanplus®)
Introducción
Tramadol/Dexketoprofeno (TR/DEX) es un fármaco que resulta de la combinación de dos analgésicos con diferente mecanismo de acción. Tramadol es un opioide de acción central y dexketoprofeno es un antinflamatorio no esteroideo con potencia analgésica, antinflamatoria y antipirética. Dicha combinación es en dosis fijas: tramadol 75 mg y dexketoprofeno 25 mg.
Indicación
TR/DEX ha sido autorizado para el tratamiento sintomático del dolor agudo moderado-intenso en adultos y a corto plazo, cuando se requiera la combinación de ambos fármacos.
Posología
La dosis máxima recomendada de TR/DEX es de 3 comprimidos/día, administrándose con un intervalo de 8 horas como mínimo. Su indicación se restringe al período sintomático y con una duración máxima de 5 días, debiendo considerarse después el cambio a un analgésico en monoterapia si así se precisase. Debe administrarse al menos 30 minutos antes de las comidas para no retrasar su absorción y con suficiente cantidad de líquido.
Eficacia
La eficacia y seguridad del TR/DEX han sido evaluadas mediante dos ensayos clínicos (fase III, aleatorios y doble ciego) en comparación con placebo y con sus componentes en monoterapia (tramadol 100 mg y dexketoprofeno 25 mg) en pacientes con dolor agudo moderado-intenso (escala visual analógica [EVA] ≥40 mm).
TR/DEX mostró diferencias estadísticamente significativas en la variable primaria a estudio (cambio en la intensidad del dolor en las primeras 8 horas tras su administración según Sum of Pain Intensity Differences), si bien ambos ensayos muestran limitaciones, como la corta duración o el número limitado de pacientes, y presentan algunos errores de estratificación.
Seguridad y tolerabilidad
La información de seguridad, el perfil de efectos adversos y las contraindicaciones de TR/DEX derivan de sus componentes en monoterapia.
Los efectos adversos más frecuentes fueron gastrointestinales y mareos, siendo estos de intensidad leve-moderada en su mayoría.
Requiere ajuste de dosis en pacientes de edad avanzada, siendo limitada la experiencia clínica en pacientes mayores de 75 años.
Coste
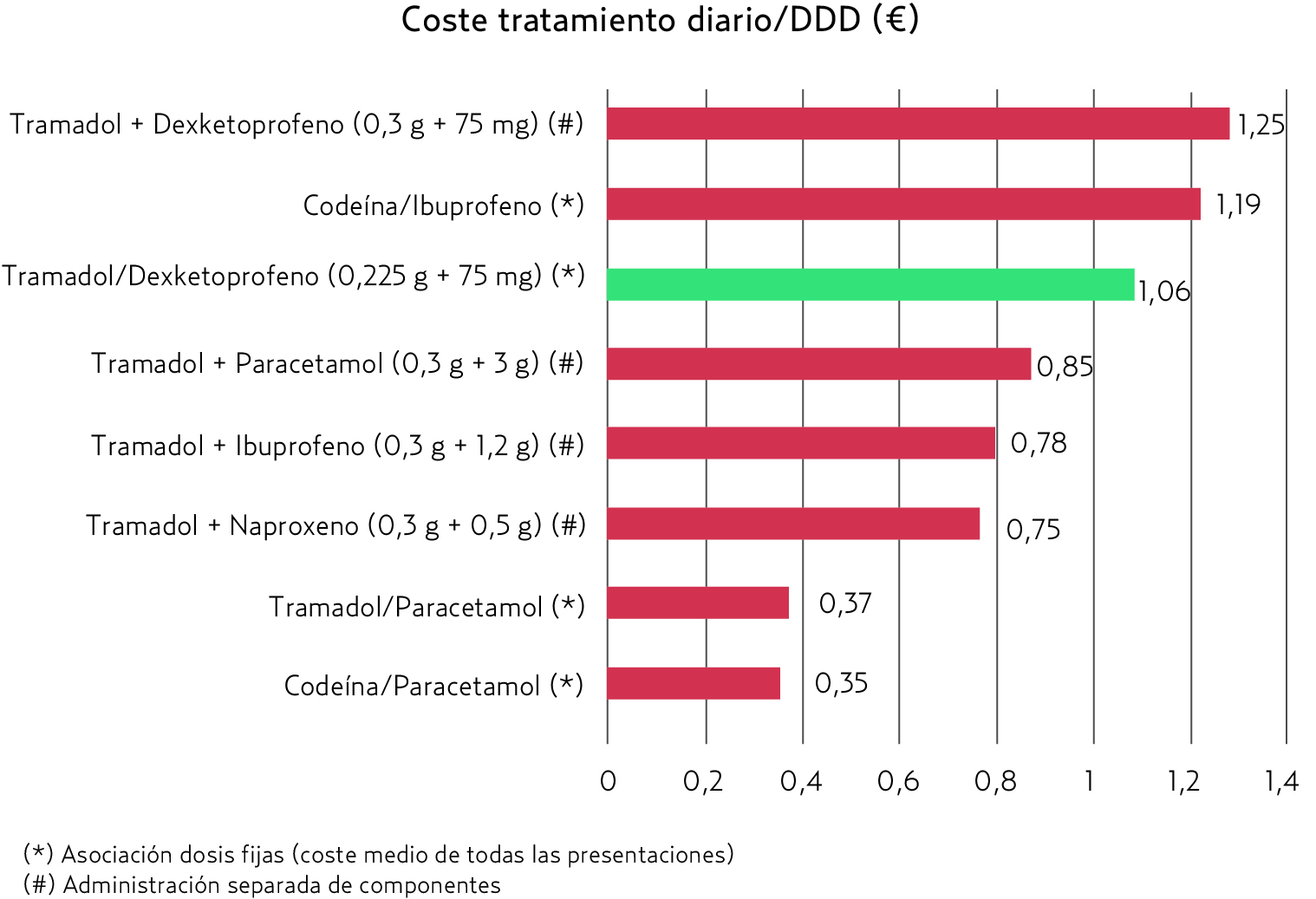
El precio de Enanplus® 20 comprimidos es de 7,10 € (figura 4).
|
Figura 4. Coste tratamiento diario/DDD (euros). Fuente: Sistema de Información FARMA. Subdirección de Prestaciones. Servicio Andaluz de Salud. Mayo 2017 |
 |
Lugar en la terapéutica
Se dispone de información insuficiente acerca de la posología, la duración terapéutica, la seguridad y la población diana. Solo existe una única presentación, lo cual puede generar dificultades a la hora de realizar el ajuste de dosis en caso de que fuese necesario. Al mismo tiempo, supone iniciar una dosis alta de tramadol (75 mg) con sus potenciales efectos adversos o intolerancia.
Los estudios realizados mostraron resultados estadísticamente significativos, pero solo analizaron el dolor posquirúrgico y no hay estudios comparativos frente a TR DEX administrados conjuntamente en diferentes preparados, frente a otras asociaciones analgésicas, ni frente a otros analgésicos en monoterapia5.
Por todo lo referido anteriormente, TR/DEX no ha supuesto un avance terapéutico en el tratamiento sintomático del dolor agudo. En la práctica clínica, se podría plantear su uso en pacientes que están tomando 75 mg/8 h de tramadol al día para reforzar el tratamiento durante unos pocos días en presencia de reagudizaciones artríticas de la artrosis.
Ampliar la información
Ficha técnica Enanplus©. https://cima.aemps.es/cima/pdfs/es/ft/80925/FT_80925.html.pdf
Alertas de seguridad farmacológica
ALERTA SOBRE ÁCIDO VALPROICO Y DAÑO FETAL
En el año 2014 se llevó a cabo una revisión del balance beneficio-riesgo de los medicamentos que contienen ácido valproico, motivada por los resultados de estudios publicados que mostraban un riesgo de trastornos en el neurodesarrollo a largo plazo en niños nacidos de mujeres tratadas con ácido valproico (hasta en un 40 % de los casos), así como por su conocido riesgo de malformaciones congénitas (en aproximadamente un 10 % de los casos).
Las medidas llevadas a cabo entonces se han reconocido insuficientes y por ello The Pharmacovigilance Risk Assessment Committee (PRAC) de la Agencia Europea de Medicamentos (EMA), tras la evaluación de los datos de utilización de los medicamentos que contienen ácido valproico, recomienda nuevas restricciones de uso y la introducción de un plan de prevención de embarazos para mujeres con capacidad de gestación:
- En niñas y en mujeres con capacidad de gestación, no se debe utilizar ácido valproico, excepto que no se pueda utilizar otra alternativa terapéutica y se cumplan las condiciones del plan de prevención de embarazos.
- En mujeres embarazadas no se debe utilizar ácido valproico en el trastorno bipolar. En caso de epilepsia solamente se podrá utilizar si no es posible otra alternativa terapéutica.
- El plan de prevención de embarazos incluye la evaluación de la posibilidad de embarazo en todas las mujeres, y el entendimiento y aceptación por parte de la paciente de las condiciones del tratamiento (que incluyen el uso de métodos anticonceptivos, pruebas de embarazo regulares y consulta con el médico en el caso de planificar un embarazo o si este ya existe). El tratamiento deberá revisarse al menos anualmente.
Ampliar la información
MUH (FV), 3/2018. Disponible en: https://www.aemps.gob.es/informa/notasInformativas/medicamentosUsoHumano/seguridad/2018/NI-MUH_FV_3-acido-valproico.htm
«Depakine, el escándalo. No podía callarme». Butlletí groc. 2018. Enero-Marzo Disponible en: https://www.icf.uab.cat/assets/pdf/productes/bg/es/bg311.18e.pdf
ALERTA SOBRE FENTANILO DE LIBERACIÓN INMEDIATA: IMPORTANCIA DE RESPETAR LAS CONDICIONES DE USO AUTORIZADAS
Fentanilo de liberación inmediata está indicado para el tratamiento del dolor irruptivo oncológico en adultos que ya reciben de forma crónica otro tratamiento de mantenimiento con opioides.
Los medicamentos de este tipo actualmente disponibles en España son los siguientes:
- Comprimidos sublinguales: Abstral®, Avaric®
- Comprimidos para chupar con aplicador integrado: Abfentiq®, Actiq®
- Película bucal soluble: Breakyl®
- Comprimidos bucales: Effentora®
- Solución para pulverización nasal: Instanyl®, Pecfent®
La información analizada muestra que el consumo global de fentanilo en España se ha incrementado en los últimos años. En el Sistema Nacional de Salud ha habido un aumento progresivo del uso de los preparados con fentanilo de liberación inmediata, habiéndose duplicado el consumo en el año 2016 con respecto al año 2010, lo que supone un uso superior al de otros países de nuestro entorno. El uso de fentanilo de liberación inmediata en el dolor no oncológico supuso más de un 40 % de los pacientes con una primera prescripción de fentanilo en Atención Primaria, en 2016. Aproximadamente, un 60 % de los casos de abuso o dependencia notificados al Sistema Español de Farmacovigilancia como sospechas de reacciones adversas se refieren a pacientes en los que fentanilo de liberación inmediata se utilizó para indicaciones no contempladas en la ficha técnica, en algunos de ellos durante periodos prolongados.
Considerando el riesgo de abuso y dependencia asociado a su uso, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) recomienda a los profesionales sanitarios:
- Respetar las condiciones de autorización de las formas de fentanilo de liberación inmediata, cuya indicación autorizada es el dolor irruptivo de origen oncológico tratado con un analgésico opioide de base.
- Valorar la necesidad del tratamiento y el uso de otras alternativas terapéuticas en pacientes que ya estén en tratamiento con fentanilo de liberación inmediata para el dolor no oncológico.
Ampliar la información
MUH (FV), 5/2018. Disponible en:https://www.aemps.gob.es/informa/notasInformativas/medicamentosUsoHumano/seguridad/2018/NI-MUH_FV_05-Fentanilo.htm
NOTA INFORMATIVA
El Ministerio de Sanidad, dentro del Plan Nacional frente a la Resistencia a los Antibióticos (PRAN), ha creado una aplicación para consultar el consumo de antibióticos en España. Es una herramienta informática que permite conocer de forma actualizada este consumo, tanto en Atención Primaria como en la Hospitalaria. Se encuentra en la web: http://www.resistenciaantibioticos.es/es. Dentro de la página inicial se encuentran los mapas de consumo.
Bibliografía
- Naloxegol for treating opioid-induced constipation. Issued: July 2015. NICE technology appraisal guidance 345. guidance.nice.org.uk/ta345. Disponible en: https://www.nice.org.uk/guidance/ta345/resources/naloxegol-for-treating-opioidinduced-constipation-82602609521605
- Home PD, Bergenstal RM, Bolli GB, Ziemen M, Rojeski M, Espinasse M, Riddle MC. Glycaemic control and hypoglycaemia during 12 months of randomized treatment with insulin glargine 300 U/mL versus glargine 100 U/mL in people with type 1 diabetes (EDITION 4). Diabetes Obes Metab. 2018 Jan;20(1):121-128.
- Concentrated insulin glargine (Toujeo) for diabetes. Med Lett Drugs Ther. 2015;57(1468):69-70.
- Roussel R, d'Emden MC, Fisher M, Ampudia-Blasco FJ, Stella P, Bizet F, et al. Glycaemic control and hypoglycaemia in people with type 2 diabetes switching from twice-daily basal insulin to once-daily insulin glargine 300 U/mL or insulin glargine 100 U/mL (EDITION 1 and EDITION 2 subgroup analysis). Diabetes Obes Metab. 2018;20(2):448-452.
- Tramadol/Dexketoprofeno. Ficha Eval Medicam. [Internet] 2017 [Consultado el 25 de febrero de 2018); (7): [2 p.] DOI: 10.11119/FEM2017-07. Disponible en: http://www.cadime.es/es/fnt.cfm?fid=136