ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Puntos clave
- Se amplía el concepto de estadio introduciendo el grado de limitación al flujo aéreo.
- Se actualiza el grado de recomendación de medidas no farmacológicas, las de menor coste y menores efectos indeseables.
- El uso de corticoides debe estar supeditado a su efectividad. Como método de evaluación de esta, se introduce el uso de la prueba terapéutica con corticoides.
- El tiotropio debe ser valorado individualmente antes de su utilización. Roflumilast tiene restringido su uso a la enfermedad pulmonar obstructiva crónica (EPOC) grave y sus limitaciones en cuanto a seguridad y no mejoría en la calidad de vida hacen que, con el conocimiento actual, no figure en las opciones terapéuticas planteadas por la guía. Indacaterol no ha demostrado ser superior a los medicamentos de su mismo grupo terapéutico.
Circunstancia: circunstancias modificantes (tipos y tratamientos alternativos):
Cambio
Circunstancia modificante-tipos
Las circunstancias modificantes se establecen en diferentes tipos según la respuesta clínica y el grado de gravedad escalonado:
• No hay mejoría.
• Disnea continua de pequeños moderados esfuerzos o síntomas nocturnos.
• Reagudización grave.
• Reagudización con criterios de infección sobreañadida en:
– EPOC leve.
– EPOC moderada-grave.
– Presencia de bronquiectasias.
• EPOC grave: hipoxemia.
Nuevos tipos de circunstancias modificantes
• EPOC leve: FEV1/FVC ≤ 70% y FEV1 ≥ 80%.
• EPOC moderada: FEV1/FVC 50-79%.
• EPOC grave o muy grave (< 30%): FEV1/FVC < 50%.
• No hay mejoría.
• Reagudización moderada o grave.
• EPOC grave. Hipoxemia.
• Reagudización con criterios de infección sobreañadida en:
– EPOC leve.
– EPOC moderada-grave.
– Presencia de bronquiectasias.
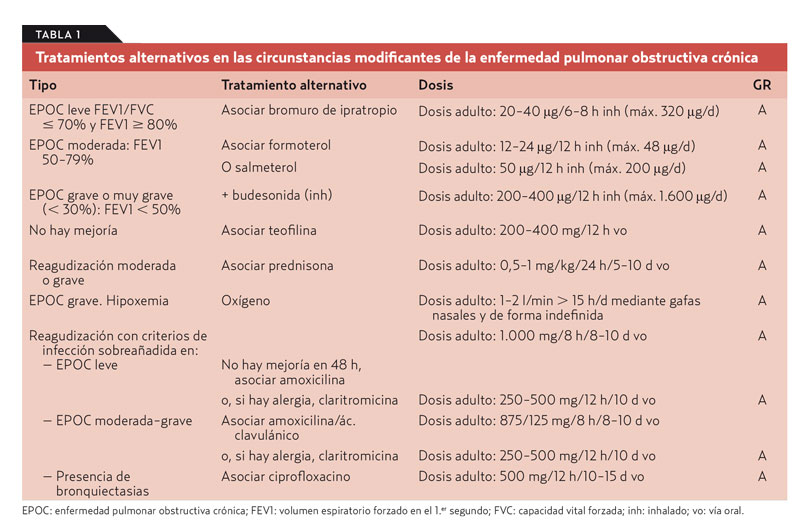
Los tratamientos alternativos que se corresponden con esta nueva relación de circunstancias modificantes se recogen en la tabla 1.
Medidas no farmacológicas
En los fumadores, el abandono del tabaco (medida fundamental) mejora la supervivencia. Si la EPOC es grave, hay que investigar si se reúnen los criterios de oxigenoterapia crónica domiciliaria (OCD) (mejora la supervivencia). (Grado de recomendación C.)
Nueva recomendación
En los fumadores, el abandono del tabaco (medida fundamental) mejora la supervivencia. (Grado de recomendación A.)
Si la EPOC es grave, investigar si se reúnen los criterios de OCD (mejora la supervivencia). (Grado de recomendación A.)
Observaciones
Eficacia de los corticoides
Los datos existentes sobre la eficacia de los corticoides en la EPOC indican que no mejoran la evolución clínica de la enfermedad. El uso de la prueba terapéutica con corticoides es controvertido.
Nueva observación
Los datos existentes sobre la eficacia de los corticoides en la EPOC indican que no mejoran la evolución clínica de la enfermedad. Antes de iniciar su prescripción, se recomienda hacer la prueba terapéutica con corticoides orales durante 14 días o inhalados durante 6 semanas. Una prueba terapéutica con corticoides se considera positiva cuando la FEV mejora en, al menos, un 15%.
Anticolinérgicos
Recientemente se ha publicado un metaanálisis que muestra un aumento del riesgo de presentar un acontecimiento cardiovascular (ACV) asociado al uso de los anticolinérgicos cuando se utilizan a largo plazo. No se ha observado, sin embargo, un incremento de la mortalidad por cualquier causa. Se recomienda, por tanto, valorar individualmente a los pacientes y hacer un seguimiento.
Nueva observación
El bromuro de tiotropio puede ser una alternativa a los broncodilatadores de larga duración beta-2-agonistas en pacientes con EPOC moderada. En diversos metaanálisis se ha sugerido que el uso de tiotropio podría asociase a un incremento en los ACV y los episodios coronarios. Esta información no se ha podido verificar en el ensayo clínico UPLIFT. Recientemente, otro metaanálisis asocia el uso de tiotropio en su nueva formulación (Respimat®) con un aumento de la mortalidad. Teniendo en cuenta esta información, se recomienda valorar individualmente a los pacientes, utilizar con precaución en pacientes con trastornos del ritmo cardíaco conocidos y no sobrepasar las dosis recomendadas.
Comentarios sobre nuevos fármacos:
Indacaterol: el Comité Mixto de Evaluación de Nuevos Medicamentos recomienda continuar utilizando el tratamiento habitual (salmeterol y formoterol) por considerar que la evidencia comparativa disponible no demuestra que tenga una eficacia superior; se desconoce su seguridad a largo plazo y su precio es mayor.
Roflumilast: es un nuevo fármaco, inhibidor de la fosfodiesterasa-4 con efecto antiinflamatorio. La indicación está restringida a los pacientes con EPOC grave (volumen espiratorio máximo por segundo [VEMS] posbroncodilatador < 50%) con frecuentes reagudizaciones como terapia adicional al tratamiento broncodilatador. Su eficacia clínica se limita a mejorar la función pulmonar y la probabilidad de exacerbaciones. No ha demostrado mejorar la calidad de vida ni disminuir los síntomas. El aumento en el número de suicidios y la disminución de peso son los aspectos más preocupantes sobre su seguridad.
Justificación
La complejidad de la EPOC genera continuas revisiones y consensos. Se trata de dar una correcta respuesta a los síntomas, evitar la progresión de la enfermedad, prevenir exacerbaciones y reducir la mortalidad.
Las medidas no farmacológicas presentan dificultades a la hora de soportar evidencia científica que las justifica debido, fundamentalmente, al poco apoyo que reciben los estudios y ensayos. Es de celebrar que en la EPOC asciendan al grado de recomendación A dos medidas no farmacológicas que mejoran la supervivencia: abandono del tabaco e investigar la existencia de criterios de OCD en los casos de EPOC grave.
El uso excesivo de corticoides inhalados en la EPOC (más del 80% en España en 2008) unido a las altas dosis empleadas hacen necesario seguir insistiendo en identificar a la población que más se puede beneficiar del tratamiento.
La aparición de nuevos fármacos obliga a sopesar su incorporación al arsenal terapéutico: un beta-2 adrenérgico de acción larga y un inhibidor de la fosfodiesterasa-4.
Lectura recomendada
Izquierdo JL, Rodríguez JM. Utilización excesiva de corticoides inhalados en la enfermedad pulmonar obstructiva crónica. Arch Bronconeumol. 2012;48:207-12.
Una evaluación de la seguridad, eficacia de dosis reducida y selección de pacientes a la hora de la utilización de corticoides en el tratamiento de la EPOC.
Bibliografía
Anónimo: Indacaterol for COPD. Drug Ther Bull.2012 may;50:58-60.
Comité de evaluación de nuevos medicamentos de Navarra. FET no 4/2012. Roflumilast (DAXAS®, LIBERTEK®) en EPOC grave. [consultado 27 de febrero de 2012]. Disponible en: URL: http://www.bit.navarra.es
Chong J, Poole P, Leung B, Black P. Inhibidores de la fosfodiesterasa 4 para la enfermedad pulmonar obstructiva crónica. Cochrane Database Syst Rev. 2011;(5):CD002309.
Global Strategy for the Diagnosis, Management and Prevention of COPD, Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2011. Disponible en: http://www.goldcopd.org/
Karner C, Chong J, Poole P. Tiotropium versus placebo for chronic obstructive pulmonary disease. Population Health Sciences and Education, St George’s, University of London, London, UK. Cochrane Database Syst Rev. 2012 Jul 11;7:CD009285.
Singh S, Loke YK, Enright PL, Furberg CD. Mortality associated with tiotropium mist inhaler in patients with chronic obstructive pulmonary disease: systematic review and meta-analysis of randomised controlled trials. BMJ. 2011;342:d3215.
Yang IA, Clarke MS, Sim EH, Fong KM. Inhaled corticosteroids for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2012 Jul 11;7:CD002991.
INFECCIÓN URINARIA
Puntos clave
- La fosfomicina trometamol en monodosis es el tratamiento de elección de la cistitis aguda en la mujer.
- En la cistitis aguda complicada, la pielonefritis aguda, la cistitis aguda en el hombre y la prostatitis aguda están indicadas pautas antibióticas largas con cultivo pretratamiento y postratamiento, y ajuste de pauta antibiótica si es necesario.
- La detección sistemática de bacteriuria asintomática se debe hacer en el embarazo, antes de la cirugía urológica y en los primeros 6 meses después de un trasplante renal.
- Es precisa la adaptación constante de la terapia antimicrobiana en función de la flora bacteriana y las resistencias antibióticas presentes en cada zona geográfica.
Circunstancia: cambio en las medidas farmacológicas, tratamiento recomendado y observaciones.
Cambio
Tratamiento recomendado
• Cistitis aguda en la mujer: fosfomicina cálcica. Dosis adulto: 500 mg/8 h/4 d vo.
• En el caso anterior, reinfección, tres o más episodios al año (sin relación con el coito): según antibiograma.
Dosis adulto: 7-14 d vo.
• Pielonefritis aguda: amoxicilina/ácido clavulánico 500 mg/125 mg/8 h/28 d vo, hasta la obtención del antibiograma. En el caso anterior, si hay intolerancia a amoxicilina/ácido clavulánico o alergia a la penicilina: ciprofloxacino. Dosis adulto: 250-500 mg/12 h/14 d.
• Prostatitis aguda: amoxicilina/ácido clavulánico 500/125 mg/8 h/28 d vo, hasta la obtención del antibiograma. En el caso anterior, si hay intolerancia a amoxicilina/ácido clavulánico o alergia a la penicilina: ciprofloxacino. Dosis adulto: 250-500 mg/12 h/28 d.
• Profilaxis de la infección urinaria de origen poscoital: nitrofurantoína. Dosis adulto: 50-100 mg/DU poscoital.
• Profilaxis de las reinfecciones: nitrofurantoína. Dosis adulto: 50-100 mg/d/6-24 m.
Observaciones
• Es conveniente conocer el patrón de resistencia en el ámbito geográfico del lugar de trabajo. Escherichia coli es uniformemente sensible a fosfomicina, por lo que esta es de elección en el tratamiento empírico de la cistitis aguda en la mujer.
• Los tratamientos en monodosis son menos eficaces que las pautas cortas de 3-5 días, y estas suelen ser tan eficaces como las pautas largas de 10 días. No obstante, la sal de trometamol de fosfomicina, administrada en dosis única de 3 g, puede ser una alternativa a la sal cálcica de fosfomicina.
• Realizar anamnesis de prurito vaginal o cambios en el flujo para hacer el diagnóstico diferencial con las vulvovaginitis. Si no hay factores de riesgo (ancianas, embarazo, inmunodeprimidos, diabetes mellitus [DM], antecedentes de pielonefritis en el último año, anomalías de las vías urinarias, instrumentación reciente de las vías urinarias, antecedentes de infección del tracto urinario [ITU] en la infancia, > 7 días de evolución de los síntomas, recaídas), no es necesario realizar urocultivo previo al tratamiento, ni tampoco sería necesario cultivo postratamiento si la evolución y la respuesta al tratamiento han sido correctas.
• Fracaso de tratamiento: urocultivo positivo a las 72 h de haber acabado el tratamiento con un antibiótico frente a germen sensible. Investigar cumplimentación e interacciones, entre otras causas.
• Recaídas: urocultivo negativo a las 72 h de haber finalizado el tratamiento, pero positivo durante las 2 semanas siguientes y frente al mismo germen (sospecha por el perfil del antibiograma). Considerar estudio urológico.
• Reinfecciones: los urocultivos a las 72 h y 15 días de haber finalizado el tratamiento son negativos.
Nueva recomendación de tratamiento
• Cistitis aguda en la mujer: fosfomicina trometamol. Dosis adulto: 3 g vo DU o norfloxacino. Dosis adulto: 400 mg/12 h/3 d vo o amoxicilina/ácido clavulánico. Dosis adulto: 500/125 mg/8 h/5 d vo. (Grado de recomendación A).
• Pielonefritis subclínica (cistitis aguda complicada) o pielonefritis aguda (sin factores de riesgo): amoxicilina/ácido clavulánico. Dosis adulto: 875/125 mg/8 h/14 d vo o ciprofloxacino. Dosis adulto: 500 mg/12 h/10-14 d vo. (Grado de recomendación A).
• Cistitis aguda en el hombre: ciprofloxacino. Dosis adulto: 250-500 mg/12 h/10-14 d o amoxicilina/ácido Clavulánico. Dosis adulto: 875/125 mg/8 h/10-14 d vo. (Grado de recomendación A).
• Prostatitis aguda: ciprofloxacino. Dosis adulto: 500 mg/12 h/21-28 d vo o amoxicilina/ácido clavulánico 875/125 mg/8 h/21-28 d vo. (Grado de recomendación A).
• Bacteriuria asintomática (en grupos de riesgo): según antibiograma. (Grado de recomendación C).
• Profilaxis de las reinfecciones: nitrofurantoína. Dosis adulto: 50-100 mg/d/6-24 m. (Grado de recomendación C).
• No hay novedades en el tratamiento de la reinfección ni en la profilaxis poscoital.
Nuevas observaciones
• Realizar anamnesis de prurito vaginal o cambios en el flujo para hacer el diagnóstico diferencial con las vulvovaginitis.
• E. colies uniformemente sensible a fosfomicina, por lo que esta es de elección en el tratamiento empírico de la cistitis aguda en la mujer. La absorción oral en ayunas de fosfomicina cálcica es del 12% (esta absorción disminuye si la fosfomicina no se administra en ayunas). La absorción de la fosfomicina trometamol es mejor (37-42% en ayunas). La eliminación urinaria de fosfomicina trometamol es del 30-60% comparado con únicamente el 9-18% de la sal cálcica. Tras la administración oral de 3 g de fosfomicina trometamol se alcanzan niveles urinarios por encima de la concentración mínima inhibitoria durante 48-72 h. La dosis única de fosfomicina trometamol es equivalente a pautas de 3 días o pautas de 5-7 días con betalactámicos, fluorquinolonas, cotrimoxazol y nitrofurantoína. La nitrofurantoína tiene un menor perfil de seguridad y una posología menos cómoda (50-100 mg/8 h/5-7 d). El cotrimoxazol tiene una tasa de resistencias superior al 20% (posología cada 12 h/3 d). Si es germen sensible, tiene una mejor penetrabilidad en tejido prostático. Por estas razones, la nitrofurantoína y el cotrimoxazol se consideran, en nuestro medio, tratamientos empíricos de segunda elección.
• Se habla de cistitis aguda complicada o pielonefritis subclínica cuando existe riesgo de colonización asintomática del riñón (ancianas, embarazo, inmunodeprimidos, DM, antecedentes de pielonefritis en el último año, anomalías de las vías urinarias, instrumentación reciente de las vías urinarias, antecedentes de ITU en la infancia, más de
7 días de evolución de los síntomas, recaídas). En este caso, la duración de este debe ser de 14 días, y es necesario realizar un cultivo pretratamiento y postratamiento. El ciprofloxacino, a diferencia de la amoxicilina/ácido clavulánico, preserva mejor las floras intestinal y vaginal. Se recomienda la dosis de amoxicilina/ácido clavulánico (875/125 mg) dada la evolución de las concentraciones mínimas inhibitorias y su mayor penetración en el tejido prostático. En caso de dificultad en la deglución, valorar la administración de cefonicid (dosis adulto: 1 g/d/10-14 d im) o gentamicina (dosis adulto: 240 mg/d/10-14 d im).
• La cistitis en el hombre es una afección poco frecuente. La infección urinaria se debería considerar un indicador de anormalidad urológica subyacente y habría que practicar una evaluación urológica. Se debe descartar siempre la uretritis, la prostatitis aguda (tacto rectal doloroso), la prostatitis crónica y la anomalía urológica. Son criterios de sospecha de cistitis no complicada: homosexualidad con relaciones anales, pacientes no circuncidados, sondaje reciente y aquellos casos en que la pareja sexual está colonizada por patógenos urinarios. Si no hay afectación del estado general, se instaurará tratamiento ambulatorio y se realizará un urocultivo posterior.
• En la prostatitis aguda se debe valorar el cambio a ciprofloxacino o cotrimoxazol, si el antibiograma informa de que el germen es sensible, dada su mejor penetrabilidad en el tejido prostático.
Se han propuesto también como profilaxis de las reinfecciones: cotrimoxazol (medio comprimido al día ([40/400 mg]), norfloxacino (400 mg/d), ciprofloxacino (100 mg/d), cefalexina (250 mg/d) o fosfomicina trometamol (3 g cada 3 d); período de toma durante 6-24 meses.
• El significado clínico de la presencia de leucocituria asociado a bacteriuria asintomática es desconocido. Recuentos muy elevados pueden persistir durante años sin que el paciente desarrolle síntomas urinarios. La bacteriuria asintomática puede causar complicaciones graves en niños < 5 años, especialmente si presentan reflujo vesicouretral (sepsis, insuficiencia renal), en enfermos sometidos a manipulación de la vía urinaria (riesgo de bacteriemia del 25-80%), en el que se le ha practicado un trasplante renal (riesgo de sepsis y fallo del injerto, sobre todo si se asocia a complicaciones urológicas) y en neutropénicos (riesgo de sepsis). En la embarazada, la bacteriuria asintomática no tratada deriva en un 20-40% de los casos en pielonefritis, que a su vez duplica el riesgo de partos prematuros y aumenta en un 50% el riesgo de recién nacidos de bajo peso. Por todo ello, la detección sistemática de esta tiene dos indicaciones claras: antes de la cirugía urológica y en la semana 16 del embarazo.
También se recomienda su detección en los primeros 6 meses después de un trasplante renal. Sigue siendo motivo de controversia el tratamiento en pacientes con DM y con incontinencia urinaria.
Justificación
El tratamiento de la infección urinaria debe ser un proceso dinámico y abierto a constante debate debido a los cambios ecológicos que se producen en los microorganismos causados por la presión antibiótica. Es indispensable conocer el patrón de resistencia en el ámbito geográfico del lugar de trabajo.
Lectura recomendada
Andreu A, Planells I; Grupo Cooperativo Español para el Estudio de la Sensibilidad Antimicrobiana de los Patógenos Urinarios. Etiología de la infección urinaria baja adquirida en la comunidad y resistencia de Escherichia coli a los antimicrobianos de primera línea. Estudio nacional multicéntrico. Med Clin (Barc). 2008;130:481-6.
Documento sobre los agentes etiológicos más habituales y la evolución de las resistencias bacterianas en nuestra población.
Bibliografía
Grabe M, Bjerklund-Johansen TE, Botto H, Wullt B, Çek M, Naber KG, et al. Guidelines on urological infections. Arnhem, The Netherlands: European Association of Urology (EAU); [Internet]; 2011 Mar. p. 39-41. Disponible en: http://www.uroweb.org/gls/pdf/15_Urological_Infections.pdf
Lorente JA, Placer J, Salvadó M, Segura C, Gelabert-Mas A. Antibiotic resistance transformation in community-acquired urinary infections. Rev Clin Esp. 2005;205(6):259-64.
Scottish Intercollegiate Guidelines Network (SIGN). Management of suspected bacterial urinary tract infection in adults. Edinburgh: SIGN [Internet]; 2012. (SIGN publication no. 88). [July 2012]. Disponible en URL: http://www.sign.ac.uk/pdf/sign88.pdf
Zalmanovici Trestioreanu A, Green H, Paul M, Yaphe J, Leibovici L. Antimicrobial agents for treating uncomplicated urinary tract infection in women. Cochrane Date Base Syst Rev. 2010 Oct 6;(10):CD007182.
INFECCIÓN URINARIA EN EL EMBARAZO
Puntos clave
- Tanto la infección urinaria sintomática como la bacteriuria asintomática en la mujer gestante están relacionadas con un riesgo aumentado de pielonefritis aguda al final del embarazo y complicaciones maternofetales (parto prematuro y bajo peso fetal).
- Deben realizarse urocultivos para descartar resistencias.
Circunstancia: cambio en el tratamiento recomendado.
Cambio
Tratamiento de elección
• Amoxicilina/ácido clavulánico. Dosis adulto: 500/125 mg/8 h/7-10 d vo.
• Intolerancia a amoxicilina/ácido clavulánico o alergia a la penicilina: fosfomicina cálcica. Dosis adulto: 500 mg/8 h/7 d vo.
• Bacteriuria asintomática: amoxicilina/ácido clavulánico. Dosis adulto: 500/125 mg/8 h/7 d vo.
Nuevas recomendaciones
• Amoxicilina/ácido clavulánico. Dosis adulto: 500/125 mg/8 h/5 d vo. (Grado de recomendación A).
• Intolerancia a amoxicilina/ácido clavulánico o alergia a la penicilina: fosfomicina cálcica. Dosis adulto: 500 mg/8 h/7-10 d vo. (Grado de recomendación A).
• Bacteriuria asintomática: según antibiograma.
Justificación
• La detección sistemática de una infección urinaria en la embarazada debe realizarse en la semana 16 del embarazo. La pauta antibiótica más corta (pasa de 10 a 5 días) tiene un grado de recomendación A. En la cistitis y la recurrencia se debe solicitar cultivo postratamiento.
• En la bacteriuria asintomática se realizará un urinocultivo 1 semana después de haber finalizado el tratamiento. Si la orina es estéril, se realizarán urinocultivos mensualmente hasta el final del embarazo. En un 20-30% de los casos la bacteriuria persistirá; en estos, se indicará la administración de un antibiótico según el antibiograma durante 7-14 días. Si la paciente sigue con bacteriuria, se debe administrar tratamiento profiláctico hasta el momento del parto con nitrofurantoína (50-100 mg vo) o cefuroxima axetilo (250 mg por la noche) previo cultivo para detectar posibles resistencias.
Lectura recomendada
Martín JC. Infecciones urinarias complicadas: revisión y tratamiento. Información Terapéutica del Sistema Nacional de Salud. [Internet]. 2004;28(6);137-44. Disponible en: http://www.msc.es/biblioPublic/publicaciones/docs/vol28_6infecciones.pdf. Incluye pautas para la detección, el manejo y el seguimiento de la infección urinaria en la gestante.
Bibliografía
Andreu A, Planells I; Grupo Cooperativo Español para el Estudio de la Sensibilidad Antimicrobiana de los Patógenos Urinarios. Etiología de la infección urinaria baja adquirida en la comunidad y resistencia de Es-cherichia coli a los antimicrobianos de primera línea. Estudio nacional multicéntrico. Med Clin (Barc). 2008;130:481-6.
Vázquez JC, Abalos E. Treatments for symptomatic urinary tract infections during pregnancy. Cochrane Data Base Syst Rev. 2011 Jan 19.
Scottish Intercollegiate Guidelines Network (SIGN). Management of suspected bacterial urinary tract infection in adults. Edinburgh: SIGN [Internet]; 2012. (SIGN publication no. 88). [July 2012]. Disponible en URL: http://www.sign.ac.uk/pdf/sign88.pdf
Protocolo SEGO: Infección urinaria y embarazo. Información terapéutica del Sistema Nacional de Salud. [Internet]. 2005;29(2). Disponible en: http://www.msps.es/biblioPublic/publicaciones/docs/vol29_2InfecUrinariaEmbarazo.pdf