|
Caso clínico |
|
Mujer, de 60 años de edad, con antecedentes de hipertensión arterial, hipercolesterolemia e hipotiroidismo en tratamiento farmacológico, y síndrome de apnea del sueño en tratamiento con CPAP (siglas en inglés de presión positiva continua en la vía aérea).
Consulta por dolor y debilidad muy limitante en la cintura escapular y pélvica, asociada a rigidez de predominio matutino, de unos 3 meses de evolución.
Niega cefalea, claudicación mandibular, trastornos visuales, fiebre, artritis periférica o síndrome constitucional.
Se le realiza una analítica sanguínea, con los siguientes resultados: velocidad de sedimentación globular (VSG) de 120 mm/h, proteína C reactiva (PCR) de 3 mg/dL con biología hepática, hemograma normal y factor reumatoide negativo.
Se inicia tratamiento con prednisona 25 mg cada 24 horas, con mejoría clínica significativa en las primeras 48 horas. |
Puntos clave
- La polimialgia reumática (PMR) es una enfermedad reumática inflamatoria que cursa con dolor y rigidez en la cintura escapular y pélvica, y suele afectar a la población mayor de 50 años.
- La arteritis de células gigantes (ACG) es una vasculitis sistémica granulomatosa que afecta a los vasos de mediano y gran calibre.
- Se desconoce la etiología de la PMR, pero varias teorías apuntan a que tiene una base genética o ambiental.
- El diagnóstico de la PMR es fundamentalmente clínico, se han definido unos criterios de clasificación que lo facilitan.
- La biopsia de la arteria temporal se considera la prueba de referencia para el diagnóstico de ACG.
- La presencia de cefalea, episodios de claudicación mandibular o amaurosis fugaz en pacientes con diagnóstico de PMR obliga a realizar una biopsia de la arteria temporal.
- El tratamiento inicial recomendado para la PMR son los glucocorticoides (GC), recomendándose iniciar el tratamiento con la mínima dosis eficaz.
- Ante la sospecha de ACG, debe iniciarse el tratamiento con GC de forma inmediata sin demorar el inicio a la confirmación diagnóstica.
- Los pacientes con sospecha ACG con síntomas visuales o isquémicos deben ser remitidos a urgencias del hospital para realizar las exploraciones pertinentes e iniciar el tratamiento con GC endovenoso.
- El seguimiento de la PMR se realizará según la clínica, los hallazgos en la exploración física y las pruebas de laboratorio (VSG y PCR).
- En cada visita se evaluarán los síntomas de PMR y de ACG, y es muy importante que el paciente haya sido previamente instruido para su detección precoz.
- En el manejo de la PMR y la ACG es muy importante la prevención y el seguimiento de los efectos secundarios de la terapia.
Concepto1,2
La polimialgia reumática (PMR) es una entidad de origen inflamatorio, de etiología desconocida, que se caracteriza por la presencia de dolor e impotencia funcional en la cintura escapular y pélvica, asociada a rigidez de predominio matutino. Suele afectar a la población mayor de 50 años y predomina en el sexo femenino. En ocasiones puede ir acompañada de síntomas constitucionales, como malestar, astenia, fatiga, fiebre, anorexia o pérdida de peso. Se puede presentar de forma aislada o asociada a ACG. Se estima que un 20% de los pacientes con PMR presentan ACG y entre un 40 y un 60% de los pacientes con ACG presentan clínica de PMR asociada, pudiendo ser incluso la forma de presentación inicial3.
La arteritis de células gigantes (ACG) es una vasculitis sistémica granulomatosa que afecta a vasos de mediano y gran calibre, sobre todo a la carótida y sus ramas principales. La sintomatología de la ACG deriva de la clínica isquémica secundaria a la arteritis. Suele presentarse como cefalea, de localización característicamente temporal, que interfiere en el sueño y es refractaria al tratamiento analgésico, pudiéndose asociar a alteraciones sensitivas del cuero cabelludo. Los pacientes afectados pueden presentar claudicación mandibular o alteraciones visuales (un 6% diplopía transitoria y hasta un 15% amaurosis fugaz o pérdida transitoria de la visión). La pérdida de algún grado de visión de forma permanente ocurre en, aproximadamente, un 20% de los casos como consecuencia de la oclusión de las arterias ciliares posteriores, de la arteria central de la retina o de infartos coroideos. La mitad de los pacientes presentan manifestaciones sistémicas (fiebre o síndrome constitucional) durante el curso evolutivo.
La incidencia de estas patologías aumenta con la edad y varía según la distribución geográfica. En un estudio realizado en España la incidencia anual para PMR fue de 13,5/100.000 habitantes, y de 18,7/100.000 habitantes para la PMR asociada a la ACG4.
Etiopatogenia1,5
Se desconoce la etiología de la PMR, pero varias teorías apuntan a una base genética o ambiental.
Teorías no demostradas apoyan que la causa podría estar relacionada con agentes infecciosos como pueden ser los adenovirus, el virus sincitial respiratorio, el parvovirus B19, Mycoplasma pneumoniae o Chlamydia pneumoniae.
En lo relacionado con los factores genéticos, varias teorías sustentan la asociación con el antígeno leucocitario humano (HLA) DR4, el gen HLA DRB1 y con polimorfismos genéticos de la molécula de adhesión celular 1 (CAM1) y las interleucinas 1 (IL-1) y 6 (IL-6).
La fisiopatología de la PMR se debe a un estado de activación del sistema inmunitario que genera un estado proinflamatorio y produce cambios a nivel hepático, hematológico y del sistema nervioso. Todo ello se traduce en las alteraciones analíticas y los síntomas constitucionales que acompañan a esta patología (anemia, leucocitosis, trombocitosis, elevación de la fosfatasa alcalina, proteína C reactiva, fibrinógeno, fiebre, mialgias, anorexia...).
 Criterios diagnósticos
Criterios diagnósticos
Polimialgia reumática
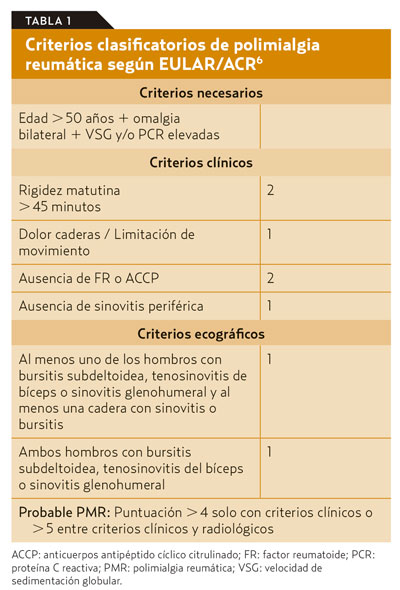
En 2012, la Liga Europea Contra el Reumatismo (EULAR) y el Colegio Americano de Reumatología (ACR)6 desarrollaron los criterios de clasificación para la PMR. Estos criterios están concebidos como una herramienta de ayuda al profesional clínico en la distinción de la PMR del resto de patologías que conforman su amplio diagnóstico diferencial y no como criterios diagnósticos7.Se detallan en la tabla 1.
Arteritis de células gigantes
Los criterios clasificatorios para la ACG fueron descritos en 1990 por el American College of Rheumatology8 y se detallan en la tabla 2. La presencia de tres o más criterios ofrece una sensibilidad del 93,5% y una especificidad del 91% para el diagnóstico de ACG.

La aparición de cefalea, episodios de claudicación mandibular o amaurosis fugaz en pacientes con PMR obliga a realizar una biopsia de la arteria temporal. En un 60% de los pacientes con criterios clínicos para ACG la biopsia es negativa9, debido a la naturaleza focal y segmentaria de la vasculitis, así como a la posibilidad de que la ACG afecte a otros vasos. En estos casos, la biopsia de la arteria contralateral mejora el diagnóstico en un 5-15%. La EULAR10 recomienda considerar la realización de una biopsia de la arteria temporal contralateral en casos seleccionados de alta sospecha clínica. Los rasgos clínicos que se asocian con mayor frecuencia a una biopsia positiva son la presencia de claudicación mandibular, diplopía o alteración visual, los cambios en la arteria temporal, la presencia de hipersensibilidad del cuero cabelludo y síndrome constitucional.
Diagnóstico diferencial de ambas patologías5,11,12
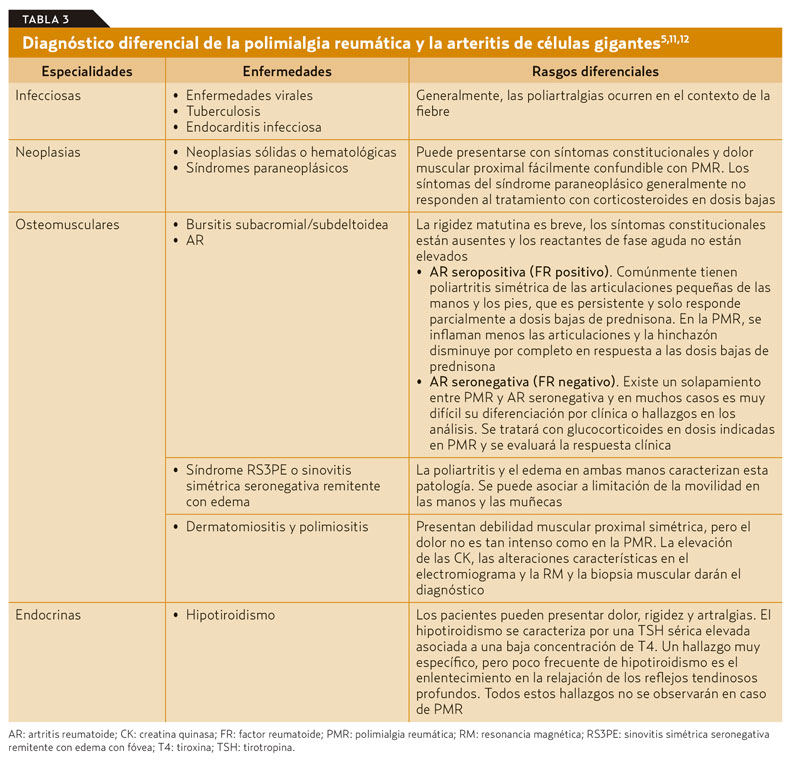
Un gran número de patologías de muy diversa índole pueden presentarse de forma similar a la PMR o a la ACG, y se muestran en la tabla 3.
¿Es necesario realizar exploraciones complementarias? ¿Cuáles?1,2,5,11,12
Polimialgia reumática
El diagnóstico es fundamentalmente clínico. Ante la sospecha de PMR, se iniciará tratamiento con GC, objetivándose una rápida respuesta en las primeras 24-72 horas, hecho que apoyará la hipótesis diagnóstica.
La finalidad de las exploraciones complementarias es confirmar la sospecha, descartar las patologías que conforman el diagnóstico diferencial y detectar, evaluar y seguir las comorbilidades o complicaciones que pueda ocasionar el tratamiento.
Ante la sospecha clínica de PMR se solicitará una analítica con hemograma completo, VSG, PCR, glucosa, función renal y hepática. Según la clínica y los hallazgos de la exploración, el clínico puede plantearse otros diagnósticos compatibles, expuestos en el apartado «Diagnóstico diferencial», precisando ampliar el estudio analítico según sus sospechas: TSH, calcio y vitamina D, creatina quinasa (CK), factor reumatoide, anticuerpo antipéptido citrulinado cíclico (ACCP), anticuerpos antinucleares (ANA), proteinograma.
A priori, las pruebas de imagen no son necesarias para alcanzar el diagnóstico de PMR, pero pueden ayudar en caso de duda. Los hallazgos ecográficos más consistentes para la PMR son la tenosinovitis del tendón largo del bíceps, la bursitis subacromial bilateral y la bursitis trocantérea. La resonancia magnética (RM) y el PET/TC (tomografía por emisión de positrones/tomografía computarizada) detectan estos mismos hallazgos aumentando su sensibilidad pero con un coste mucho más elevado. En una PMR se planteará la solicitud de un estudio PET/TC en aquellos pacientes con sospecha de vasculitis asociada (ausencia de respuesta al tratamiento con GC, niveles elevados persistentes de VSG o PCR o síndrome constitucional muy marcado).
Arteritis de células gigantes
La biopsia de la arteria temporal se considera la prueba de referencia; una biopsia positiva confirma el diagnóstico, pero una biopsia negativa no puede descartarlo debido a la naturaleza focal y segmentaria de esta patología y a la posibilidad de que no siempre afecte a esta localización. Un resultado normal de ambas biopsias temporales confiere un valor predictivo negativo para ACG superior al 90%. La biopsia en esta arteria se ha elegido por su fácil accesibilidad anatómica y por la frecuente afectación en la ACG. Se realizará en el lado con mayor afectación clínica y debe extraerse una muestra de entre 3 y 5 cm para mejorar el rendimiento diagnóstico. Los hallazgos histopatológicos característicos son los de una panarteritis focal con presencia de granulomas, células gigantes multinucleadas y destrucción de la lámina elástica interna y de la capa muscular.
La ecografía Doppler de la arteria temporal es una técnica no invasiva, altamente coste-efectiva y accesible que se utiliza para evaluar la inflamación vascular de las arterias temporales, así como estenosis y oclusiones. Un hallazgo típico en la AGC es el «signo halo», anillo hipoecoico alrededor de la luz arterial que representa el engrosamiento edematoso que produce la inflamación. Estaría indicada cuando no se pueda hacer una biopsia, presentando una sensibilidad del 75% y una especificidad del 83% respecto a la biopsia de la temporal.
Ante la sospecha de una vasculitis de grandes vasos en la ACG, se solicitará un estudio angiográfico mediante TC o RM para valorar la aorta y sus principales ramas. Otra de las exploraciones complementarias emergentes que pueden ser de utilidad ante esta sospecha es el PET/TC, que se puede indicar en aquellos pacientes que no responden adecuadamente al tratamiento con GC, en los que persisten marcadores inflamatorios elevados, a pesar del tratamiento o en aquellos pacientes con manifestaciones atípicas de ACG, como cuadro constitucional, fiebre o claudicación de las extremidades superiores.
Tratamiento
Polimialgia reumática
El objetivo del tratamiento es la desaparición de los síntomas y la inflamación, restaurando el nivel de funcionalidad que el paciente presentaba antes del episodio11; no mejora el pronóstico de la enfermedad ni previene la progresión a ACG13.
El tratamiento inicial recomendado para la PMR son los GC, con una eficacia establecida desde hace décadas por la amplia experiencia clínica y los estudios observacionales publicados. Pese a esto, no hay un enfoque universalmente aceptado sobre la dosis de inicio y manejo, y la praxis se rige por las guías de práctica clínica publicadas14,15 y la revisión de expertos13,16.
Se recomienda iniciar el tratamiento con la mínima dosis eficaz de GC (12,5-25 mg/día de prednisona o equivalente), que puede variar en función del peso del paciente o la intensidad de los síntomas13. La respuesta suele aparecer a las 24-72 horas del inicio.
La reducción de la dosis ha de ser individualizada. Se recomienda que tras la resolución de los síntomas y la inflamación (corrección de los reactantes de fase aguda), normalmente unas 4 semanas después del inicio, se disminuya progresivamente a una dosis de 10 mg/día de prednisona o equivalente en un intervalo de unas 4-8 semanas. Posteriormente se reduce 1 mg mensual hasta su retirada.
Las recaídas durante la reducción del tratamiento son frecuentes, sobre todo cuando el paciente se maneja con dosis < 10 mg/día17, aunque también suceden meses o años después de la finalización del tratamiento18. Los factores de riesgo de recaída se detallan en la tabla 4.
En caso de presentar recaída durante la reducción, se aumentaran los GC en la dosis previa con la que se controlaba la sintomatología para, posteriormente, realizar una reducción gradual más lenta (en un período de 4-8 semanas) hasta alcanzar la dosis con la que se presentó14.
En ocasiones, debido a las comorbilidades del paciente, la respuesta incompleta del tratamiento con GC o sus efectos secundarios, se debe plantear la introducción de otros fármacos normalmente de forma coadyuvante. Estos factores se detallan en la tabla 5.
En estos supuestos se considerará la introducción temprana de metotrexato en dosis de 7,5-10 mg/semanales14 o tocilizumab (anti-interleucina-6 receptor). Este último estaría indicado en pacientes que no responden al tratamiento con corticoides y metotrexato o en quienes su uso está contraindicado. Es un tratamiento aprobado en Estados Unidos para la ACG, pero aún no tiene la aprobación para la PMR aislada11.
El manejo de estos fármacos se realizará por parte de profesionales con experiencia en su uso, quedando fuera de la práctica habitual del médico de familia.


Arteritis de celulas gigantes o arteritis de Horton
Un porcentaje no despreciable de los pacientes con PMR presentan ACG asociada (10-15%). Ante la sospecha de ACG, debe iniciarse el tratamiento con GC inmediatamente, sin demorar el inicio a la confirmación diagnóstica, ya que el tratamiento con GC mejora los síntomas de forma precoz y previene la aparición de neuritis óptica isquémica arterial, la complicación más grave de esta enfermedad. El inicio precoz no altera los hallazgos histopatológicos de la biopsia de la arteria temporal, que permanecen presentes durante semanas12,19,20.
El manejo se basa en las recomendaciones de expertos y las guías de práctica clínica12:
- Si el paciente no presenta alteración visual en el momento de la sospecha diagnóstica, se recomienda administrar prednisona o equivalente en dosis de 1 mg/kg/día (máximo 60 mg/día) administrada en dosis única. Tras 4 semanas, se iniciará el descenso a un ritmo del 10-20% cada 2 semanas hasta dosis de 10 mg/día, donde la reducción se continuará a ritmo de 1 mg/mes12,19. La mayoría de las recaídas aparecen durante el primer año de tratamiento cuando la dosis de prednisona se ha reducido a menos de 20 mg/día. Se suele manifestar con la aparición de cefalea o síntomas de PMR.
- Si el paciente presenta clínica visual, se le remitirá a urgencias del centro hospitalario de referencia para iniciar tratamiento con metilprednisolona endovenosa en dosis de 500-1.000 mg/día durante 3 días para, posteriormente, pasar a prednisona por vía oral en dosis de 60 mg/día.
- En pacientes con ACG refractaria a GC o con efectos secundarios o comorbilidades que limiten su uso puede plantearse el tratamiento con metotrexato y tocilizumab asociado, que facilitan la reducción de recidivas y la dosis acumulada de GC11.
Seguimiento y duración del tratamiento
Polimialgia reumática
Tras el inicio del tratamiento con GC, se recomienda un control clínico, presencial o telefónico, para comprobar la respuesta que habitualmente suele ser muy rápida y significativa (24-72 horas). La ausencia de respuesta obliga a replantear el diagnóstico.
Se ha consensuado realizar un seguimiento clínico cada 4-8 semanas durante el primer año de tratamiento y posteriormente cada 8-12 semanas para observar la evolución y valorar las posibles complicaciones del tratamiento3,11.
El seguimiento se realizará según la clínica, los hallazgos en la exploración física y las pruebas de laboratorio (VSG y PCR). En cada visita se evaluarán los síntomas de PMR y de ACG, y es muy importante que el paciente haya sido previamente instruido para su detección precoz.
La monitorización de la VSG y la PCR se realizará en el momento del diagnóstico y posteriormente de forma seriada cada 4-8 semanas durante los primeros 3-6 meses. Si el paciente se encuentra asintomático, se espaciarán los controles analíticos cada 3 meses. En caso de reaparición de síntomas sugerentes de recaída, también se solicitarán11.
Durante el seguimiento analítico, la elevación persistente de la PCR se asocia a un aumento del riesgo de recaída durante el primer año13; la PCR es más sensible y se ajusta más al grado de actividad de la enfermedad que la VSG2. La persistencia de valores muy elevados de VSG o PCR o su aumento en pacientes asintomáticos con el tratamiento obliga a descartar una ACG u otras enfermedades concomitantes13.
Un 50% de los pacientes finalizan el tratamiento tras 1-2 años, otros precisan dosis continuas de GC durante períodos más prolongados, los factores que suelen asociarse son el sexo femenino, la presencia de artritis periférica y una VSG muy elevada14.
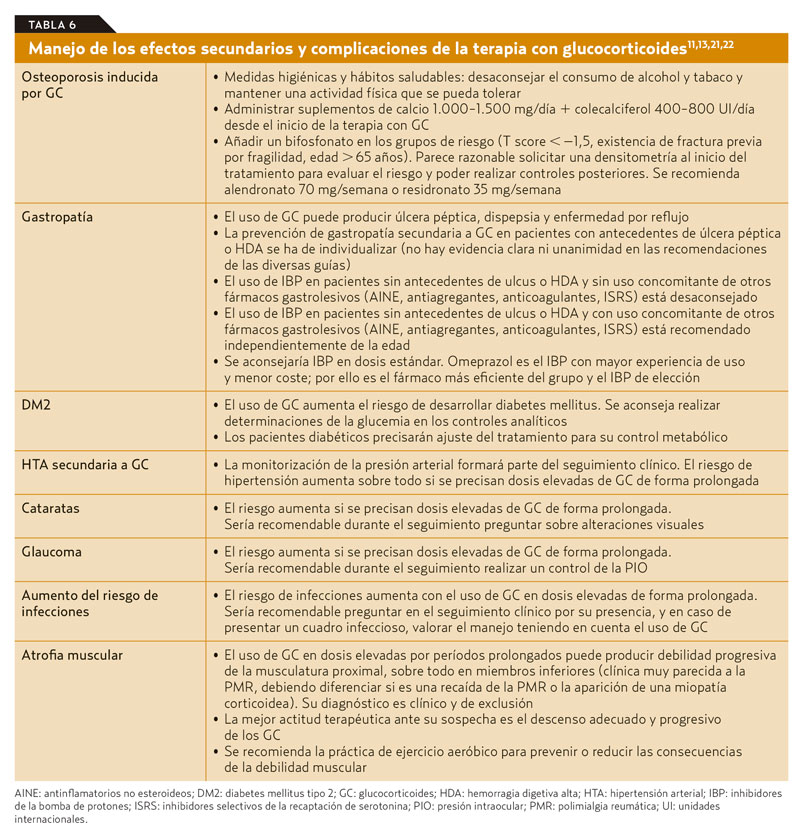
En la PMR son frecuentes las recaídas y la corticodependencia, observándose efectos secundarios relacionados con la terapia en un 43-65% de los pacientes según las series14. Su prevención y control forman parte del seguimiento clínico de la PMR y se detallan en la tabla 611,13,21,22.
El manejo y seguimiento de los pacientes con PMR tratados con metotrexato se realiza en las consultas de reumatología, pero el médico de Atención Primaria debe estar familiarizado con sus efectos. El metotrexato es hepatotóxico, por lo que desde AP se desaconsejará el consumo de alcohol y se vigilará la conciliación farmacológica. Puede producir estomatitis oral y enfermedad intersticial pulmonar (la presencia de tos, disnea o cambios en la auscultación puede indicarlo).
En el seguimiento de la PMR se aconseja la intensificación del control de los factores de riesgo cardiovascular (FRCV) no tan solo por el empeoramiento secundario al tratamiento con GC descrito en la tabla 6, sino por el aumento del RCV evidenciado durante los primeros meses tras el diagnóstico, sobre todo en pacientes menores de 60 años23.
Arteritis de células gigantes o arteritis de Horton12,13,24
El seguimiento de los pacientes con PMR asociada a ACG debe ser controlado por el servicio de Reumatología o medicina interna de referencia, aunque el médico de AP debe estar familiarizado con su manejo y aprovechar las visitas con el paciente para instruirlo en la detección precoz de los síntomas de recaída, detectar posibles complicaciones de la enfermedad y del tratamiento y valorar la adherencia terapéutica así como su conciliación. El seguimiento consiste en:
- Seguimiento clínico del paciente. El intervalo de visitas, analíticas y el descenso de la dosis de GC se individualizará en función de la evolución clínica. Su tratamiento suele mantenerse entre 1-2 años. Las recaídas son frecuentes, sobre todo cuando la dosis de GC es < 20 mg/día. Los pacientes en remisión crónica que presenten recidiva deben ser tratados como al inicio del diagnóstico; si la recaída se presenta con sintomatología sugestiva de PMR durante la reducción del tratamiento, un aumento de la dosis de 5-7,5 mg/día suele ser suficiente. En el caso de presentar clínica oftálmica o neurológica, se remitirá a urgencias para administrar tratamiento endovenoso.
- Prevención y control de los efectos secundarios del tratamiento farmacológico. Según las series, un 86% de los pacientes experimentan por lo menos un efecto adverso a lo largo del tratamiento. Estos efectos y su manejo se detallan en el apartado de «Seguimiento y duración del tratamiento» y en la tabla 6. Destacar el aumento del riesgo de sufrir infecciones oportunistas, sobre todo en los primeros 6 meses de tratamiento donde las dosis de GC son más elevadas.
- Control y prevención de las complicaciones intrínsecas a la ACG. Los pacientes con ACG pueden presentar estenosis de la arteria subclavia y axilar (10-15%), aneurisma de aorta (su incidencia tras el diagnóstico supera el 30%, siendo la localización torácica la más frecuente), pérdida de visión (el riesgo de aparición habiendo iniciado el tratamiento es del 1% y el de progresión habiendo presentado sintomatología previa al inicio del tratamiento, del 13%) y enfermedades cardiovasculares (se ha demostrado que la presencia de ACG puede aumentar el riesgo de padecerlas).
¿Cuándo derivar?
El médico de AP debe considerar la derivación al servicio de reumatología en caso de:
- PMR de presentación atípica (presencia de fiebre, pacientes jóvenes).
- Falta de respuesta al tratamiento con GC.
- Comorbilidades o efectos adversos que limiten el uso de GC.
- Recaídas frecuentes durante la reducción de la dosis de GC.
- Cuadro clínico con predominio de artritis periférica que requiere un diagnóstico diferencial con artritis seronegativas o artritis reumatoide de inicio tardío.
- Toda PMR con sospecha de ACG asociada.
En el caso de sospechar ACG con síntomas visuales u otros síntomas isquémicos, se remitirá al paciente al servicio de urgencias de referencia para la administración intravenosa de GC y para el seguimiento clínico y metabólico pertinente, así como para realizar las exploraciones complementarias necesarias.
Lecturas recomendadas
Weinreb A. Polymyalgia Rheumatica. BMJ Best Practice [sede Web]. London: BMJ Publishing Group Limited 2018. [Last updated: Jun 6, 2018, acceso 23/05/2019]. Disponible en: http://bestpractice.bmj.com/topics/en-us/153
Warrington KJ. Giant cell arteritis. BMJ Best Practice [sede Web]. London: BMJ Publishing Group Limited 2018. [Last updated: Dec 12, 2018, acceso 23/05/2019]. Disponible en: http://bestpractice.bmj.com/topics/en-gb/177
Dos lecturas que resumen, de forma clara y concisa, estas patologías y esquematizan muy bien su abordaje. Muy buen punto de partida para actualizarnos sobre la PMR y la ACG. Ha sido el pilar sobre el que se ha basado nuestro artículo.
Bibliografía
- Ventura Valcárcel P, Romay Lema E, Iñiguez Vázquez I, Rubal Bran D, Lorenzo López M, Piñeiro Fernández JC. Guía clínica de Polimialgia reumática. Fisterra.com Atención Primaria en la Red [sede Web]. La Coruña: Fisterra.com; 1990 [Actualizada el 16/12/2016; acceso el 18/5/2019]. Disponible en: https://fisterra.com/guias-clinicas/polimialgia-reumatica/
- Romay Lema E, Ventura Valcárcel P, Íñiguez Vázquez I, Pedrosa Fraga C, Suárez Gil R, López Díaz MJ. Guía clínica de Arteritis de células gigantes. Fisterra.com Atención Primaria en la Red [sede Web]. La Coruña: Fisterra.com; 1990 [Actualizada el 30/11/2017; acceso el 12/06/2019]. Disponible en: https://www.fisterra.com/guias-clinicas/arteritis-celulas-gigantes/
- González-Gay MA, Pina T. Giant cell arteritis and polymyalgia rheumatica: an update. Curr Rheumatol Rep. 2015;17(2):6.
- González-Gay MA, Vázquez Rodríguez TR, López Diaz MJ, Miranda Filloy JA, González Juanatey C, Martín J, Llorca J. Epidemiology of giant cell arteritis and polymyalgia rheumatica. Arthritis Rheum. 2009;61(10):1454-61.
- Docken WP. Clinical manifestations and diagnosis of polymyalgia rheumatica [sede Web]. [Last update: 02/11/2017; acceso 18/05/2019]. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. https://www.uptodate.com/contents/clinical-manifestations-and-diagnosis-of-polymyalgia-rheumatica
- Dasgupta B, Cimmino MA, Maradit-Kremers H, Schmidt WA, Schirmer M, Salvarani C, et al. 2012 Provisional classification criteria for polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology collaborative initiative. Arthritis Rheum. 2012;64:943.
- Aggarwal R, Ringold S, Khanna D, Neogi T, Johnson SR, Miller A, et al. Distinctions between diagnostic and classification criteria? Arthritis Care Res (Hoboken). 2015;67:891-7.
- Hunder GG, Bloch DA, Michel BA, Stevens MB, Arend WP, Calabrese LH, et al. The American College of Rheumatology 1990 criteria for the classification of giant cell arteritis. Arthritis Rheum. 1990;33(8):1122-8.
- Goslin BJ, Chung MH. Temporal artery biopsy as a means of diagnosing giant cell arteritis: is there over-utilization? Am Surg. 2011;77(9):1158-60.
- Mukhtyar C, Guillevin L, Cid MC, Dasgupta B, De Groot K, Gross W, et al; European Vasculitis Study Group. EULAR recommendations for the management of large vessel vasculitis. Ann Rheum Dis. 2009;68(3):318-23.
- Weinreb A. Polymyalgia Rheumatica. BMJ Best Practice [sede Web]. London: BMJ Publishing Group Limited 2018. [Last updated: Jun 6, 2018, acceso 23/05/2019]. Disponible en: http://bestpractice.bmj.com/topics/en-us/153
- Warrington KJ. Giant cell arteritis. BMJ Best Practice [sede Web]. London: BMJ Publishing Group Limited 2018. [Last updated: Dec 12, 2018, acceso 23/05/2019]. Disponible en: http://bestpractice.bmj.com/topics/en-gb/177
- Docken WP. Treatment of polymyalgia rheumatica [sede Web]. [Last update: Sep 07, 2018; acceso 24/05/2019]. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. https://www.uptodate.com/contents/treatment-of-polymyalgia-rheumatica/print
- Dajeco C, Singh YP, Perel P, Hutchings A, Camellino D, Mackie S, et al.; European League Against Rheumatism; American College of Rheumatology. 2015 Recommendations for the management of polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology Collaborative Initiative. Arthritis Rheum. 2015 Oct;67(10):2569-80.
- Dasgupta B, Borg FA, Hassan N, Barraclough K, Bourke B, Fulcher J, et al.; BSR and BHPR Standards, Guidelines and Audit Working Group. BSR and BHPR guidelines for the management of polymyalgia rheumatica. Rheumatology (Oxford). 2010;49:186-90.
- Hernández Rodríguez J, Cid MC, López Soto A, , Espigol-Frigolé G, Bosch X. Treatment of polymyalgia rheumatica: a systematic review. Arch Intern Med. 2009;169:1839-50.
- González-Gay MA, García Porrúa C, Vázquez Caruncho M, Dababneh A, Hajeer A, Ollier WE. The spectrum of polymyalgia rheumatica in northwestern Spain: incidence and analysis of variables associated with relapse in a 10 year study. J Rheumatol. 1999;26:1326-32.
- Docken WP. Polymyalgia rheumatica can recur years after discontinuation of corticosteroid therapy. Clin Exp Rheumatol. 2009;27(1 Suppl 52):S25-7.
- Docken WP. Treatment of giant cell arteritis [sede Web]. [Last update: Aug 13, 2018; acceso 24/05/2019]. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. https://www.uptodate.com/contents/treatment-of-giant-cell-arteritis
- Buttgereit F, Dejaco C, Matteson EL, Dasgupta B. Polymyalgia Rheumatica and Giant Cell Arteritis: A Systematic Review. JAMA. 2016;315(22):2442-58.
- Helliwell T, Hider SL, Mallen CD. Polymyalgia rheumatica: diagnosis, prescribing, and monitoring in general practice. Br J Gen Pract. 2013;63(610):e361-366.
- Osakidetza. Inhibidores de la bomba de protones: recomendaciones de uso. Boletín INFAC. [revista electrónica] 2016;24(8). [Consultado 15/06/2019]. Disponible en: https://www.osakidetza.euskadi.eus/cevime
- Hancock AT, Mallen CD, Muller S, Belcher J, Roddy E, Helliwell T, Hider SL. Risk of vascular events in patients with polymyalgia rheumatica. CMAJ. 2014;186(13):e495-501.
- Shbeeb I, Challah D, Raheel S, Crowson CS1, Matteson EL. Comparable rates of Glucocorticoid Associated Adverse Events in Patients with Polymyalgia Rheumatica and Comorbidities in the General Population. Arthritis Care Res (Hoboken). 2018;70:643-647.